
【题目】某化妆品的组分Z具有美白功效,原料从杨树中提取,现可用如下反应制备:
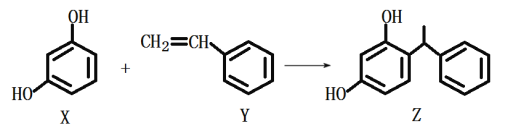
下列叙述错误的是
A. X、Y和Z均能使溴水褪色,且原理相同
B. X和Z均能与Na2CO3溶液反应放出CO2
C. Z中含手性碳原子
D. Y可作加聚反应的单体,X可作缩聚反应的单体
科目:高中化学 来源: 题型:
【题目】已知某密闭容器中存在下列平衡:CO(g)+H2O(g) ![]() CO2(g)+H2(g),CO2的平衡物质的量浓度c(CO2)与温度t的关系如图所示。下列说法错误的是 ( )
CO2(g)+H2(g),CO2的平衡物质的量浓度c(CO2)与温度t的关系如图所示。下列说法错误的是 ( )

A. 平衡状态A与C相比,平衡状态A的c(CO)较小
B. 在t2时,D点的反应速率:v(逆)>v(正)
C. 反应CO(g)+H2O(g) ![]() CO2(g)+H2(g)的ΔH>0
CO2(g)+H2(g)的ΔH>0
D. 若t1、t2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质的方法错误的是
A.除去KCl中混有的KI:溶于水通入过量氯气,蒸发结晶
B.除去BaSO4固体中混有的BaCO3:加过量盐酸后,过滤
C.除去Na2CO3固体中的NaHCO3:加热至恒重
D.除去CO2中混有的HCl:将气体通过饱和Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列化学反应和事实,说明反应利用了硫酸的什么性质,将表示性质的选项的字母填在各小题的横线上.
A.不挥发性 B.酸性 C.吸水性 D.脱水性 E.强氧化性 F 强酸性
(1)浓硫酸可作气体干燥剂___________________
(2)蔗糖中加浓![]() 产生“黑面包”现象__________________
产生“黑面包”现象__________________
(3)![]() (稀)=
(稀)=![]() _________________
_________________
(4)![]() _________________
_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】市场上有一种加酶洗衣粉,它是在洗衣粉中加入少量的碱与蛋白酶制成的。蛋白酶的催化活性很强,衣物的汗渍、血迹及入体排放的蛋白质,油渍遇到它,都能水解而除去。下列衣料中,不能用加酶洗衣粉洗涤的是:
①棉成品 ②毛织品 ③腈纶织品 ④丝织品
A.②④B.②③C.①③D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Z元素的最外层电子数是内层电子总数的1/2。下列说法不正确的是( )
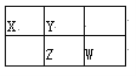
A. Z元素位于周期表的第三周期第VA族
B. X、W元素的最高价氧化物对应水化物的酸性:W强于X
C. Y元素的气态氢化物的热稳定性比Z的高
D. X与W形成共价化合物XW2, X的原子半径比Y小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在25℃、101kPa时,1gCH4完全燃烧生成液态水时放出的热量是55.64 kJ,则表示甲烷燃烧热的热化学方程式是___________________________________________。
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)===3CO2(g)+4H2O(l)
ΔH=-2 220.0 kJ· mol-1,已知CO气体燃烧的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-565.14 kJ·mol-1,试计算相同物质的量的C3H8和CO燃烧产生的热量的比值________(保留小数点后一位)。
(3)氢气既能与氮气发生反应又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ· mol-1
3H2(g)+N2(g)![]() 2NH3(g) ΔH=-92.4 kJ· mol-1
2NH3(g) ΔH=-92.4 kJ· mol-1

计算断裂1 mol N≡N键需要消耗能量________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如下图所示:
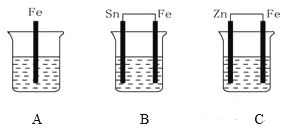
(1)A中反应的离子方程式是______。
(2)B中Sn极的电极反应式为____,Sn极附近溶液的pH____(填“增大”“减小”或“不变”)。
(3)C中被腐蚀的金属是____,总反应离子方程式是____,比较A、B、C中铁被腐蚀的速率由快到慢的顺序是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述中正确的是( )

A.图Ⅰ所示电池中,负极电极反应为Zn-2e-![]() Zn2+
Zn2+
B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C.图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中被还原为Ag
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com