
| A. | 浓的强酸和稀的强碱溶液反应 | B. | 浓的弱酸和稀的强碱溶液反应 | ||
| C. | 等pH值的强酸和弱碱溶液反应 | D. | 生成一种强酸弱碱盐 |
分析 一种0.1mol•L-1的一元酸和一种0.1mol•L-1的一元碱溶液等体积混合后,溶液呈酸性,说明反应生成了强酸弱碱盐,即:该一元酸为强酸、一元碱为弱碱,据此进行判断.
解答 解:A.浓的强酸和稀的强碱溶液反应生成强酸强碱盐,溶液为中性,不可能为酸性,且两溶液的浓度都是0.1mol/L,不会是浓的强酸,故A错误;
B.浓的弱酸和稀的强碱溶液反应生成强碱弱酸盐,溶液呈碱性,不可能为酸性,故B错误;
C.等pH值的强酸和弱碱溶液反应,混合液中酸过量,溶液呈酸性,但是弱酸只能部分电离,两溶液的浓度不会相同(0.1mol/L),与题干信息不相符,故C错误;
D.0.1mol•L-1的一元酸和一种0.1mol•L-1的一元碱溶液等体积混合后,溶液呈酸性,说明反应生成了强酸弱碱盐,故D正确;
故选D.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确弱电解质电离特点及盐的水解原理为解答关键,注意熟练掌握酸碱混合的定性判断方法.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 少量白磷贮存于水中,切割时要在水下进行 | |
| B. | 液溴直接保存于磨口玻璃塞的细口棕色瓶中 | |
| C. | KOH溶液存放在磨口玻璃塞的广口瓶中 | |
| D. | 少量金属钠存放在无水乙醇中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
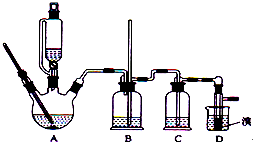 和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
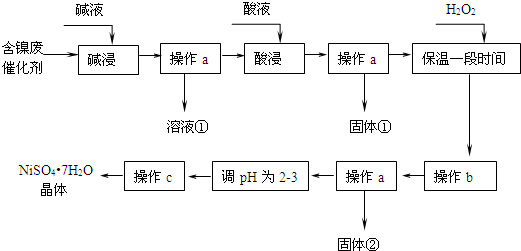
| 沉淀物 | 开始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ;
; ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
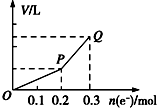 用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定).欲使溶液恢复到起始状态,可向溶液中加入( )| A. | 0.15 mol CuO | B. | 0.1 mol CuCO3 | ||
| C. | 0.075mol Cu(OH)2 | D. | 0.05 mol Cu2(OH)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸 | B. | 烧碱溶液 | C. | AgNO3溶液 | D. | KSCN溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 分离方法 | 原理 |
| A | 除去Fe(OH)3胶体中的FeCl3 | 过滤 | 分散质微粒的大小不同 |
| B | 除去纯碱中的碳酸氢铵 | 加热 | 稳定性不同 |
| C | 分离KNO3和NaCl | 重结晶 | KNO3的溶解度大于NaCl |
| D | 分离食用油和汽油 | 分液 | 食用油和汽油的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com