
| A. | 配制90mL1.00mol/L的NaCl溶液,用托盘天平称取5.3gNaCl固体 | |
| B. | 使用容量瓶时,先检验其是否漏水,然后洗净后,不用干燥即可使用 | |
| C. | 可用10mL量筒量取8.58mL蒸馏水 | |
| D. | 在配制溶液定容后,上下翻转摇匀后发现液面下降,须加水至溶液凹液面与刻度线相切 |
分析 A.配制90mL溶液,需要100mL容量瓶,结合m=cVM计算;
B.容量瓶有塞子,需要查漏,定容还需加水,则不需要干燥;
C.量筒的感量为0.1mL;
D.配制溶液定容后,上下翻转摇匀后发现液面下降,为正常现象,液体可残留在塞子处.
解答 解:A.配制90mL溶液,需要100mL容量瓶,NaCl的质量m=0.1L×1.00mol/L×58.5g/mol=5.85g,则用托盘天平称取5.8g或5.9gNaCl固体,故A错误;
B.容量瓶有塞子,需要查漏,定容还需加水,则不需要干燥,则使用容量瓶时,先检验其是否漏水,然后洗净后,不用干燥即可使用,故B正确;
C.量筒的感量为0.1mL,则用10mL量筒量取8.5mL或5.9mL蒸馏水,故C错误;
D.配制溶液定容后,上下翻转摇匀后发现液面下降,为正常现象,液体可残留在塞子处,不能再加水至溶液凹液面与刻度线相切,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液配制的仪器、步骤及操作为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
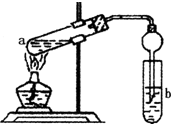 如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验.
如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
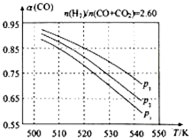 甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:| 物质 | CO | CO2 | H2 | CH3OH(g) |
| 标准生成热(kJ/mol) | -110.52 | -393.51 | 0 | -201.25 |
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |||
| CH3OH(g) | CH3OCH3(g) | H2O(g) | CH3OCH3(g) | H2O(g) | ||
| a | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
| b | 387 | 0.40 | 0 | 0 | ||
| c | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
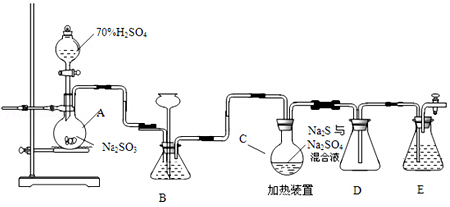
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(CO)=1.2 mol/(L•s) | B. | v(NO2)=0.3 mol/(L•min) | ||
| C. | v(N2)=0.6 mol/(L•min) | D. | v(CO2)=1.2 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
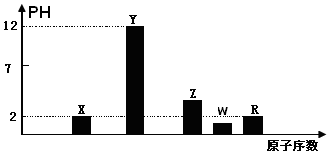


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,能与NaOH溶液反应生成盐和水 | |
| B. | 实验室中用石灰水区分Na2CO3与NaHCO3两瓶无标签溶液 | |
| C. | O3和O2为同种元素组成的单质,所以O3和O2互为同位素 | |
| D. | Na2O和Na2O2组成元素相同,与H2O的反应产物也相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com