
���� ��1������n=$\frac{N}{{N}_{A}}$���������������ʵ���������n=$\frac{V}{{V}_{m}}$���������̼�����ʵ�����
��2��������������Һ������������ʵ���Ӱ�죬�ٸ���c=$\frac{n}{V}$�жϣ�
��3��̼�����Ƽ��ȷֽ�Ϊ̼���ơ�������̼��ˮ��̼�����������ᷴӦ�����Ȼ��ơ�������̼��ˮ��
��4��Al��������������Һ��Ӧ����Mg���ܣ�
��� �⣺��1�������������ʵ���Ϊ$\frac{9.03��1{0}^{23}}{6.02��1{0}^{23}mo{l}^{-1}}$=1.5mol��������̼�����ʵ���Ϊ$\frac{11.2L}{22.4L/mol}$=0.5mol��
�ʴ�Ϊ��1.5��0.5��
��2��A�����ձ����ܽ�ʱ��������Һ����������������ƿ�����ʵ����ʵ���ƫС��������ҺŨ��ƫС��
B������ʱ�����ӿ̶��ߣ�Һ���ڿ̶����·�����Һ���ƫС��������ҺŨ��ƫ��
C��������ˮ���ݣ�ת��ʱ������ƿ��������ˮ������ҺŨ����Ӱ�죬
�ʴ�Ϊ��ƫС��ƫ����Ӱ�죻
��3��̼�����Ƽ��ȷֽ�Ϊ̼���ơ�������̼��ˮ����Ӧ����ʽΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$2Na2CO3+H2O+CO2����
̼�����������ᷴӦ�����Ȼ��ơ�������̼��ˮ����Ӧ���ӷ���ʽΪ��HCO3-+H+=H2O+CO2����
�ʴ�Ϊ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$2Na2CO3+H2O+CO2����HCO3-+H+=H2O+CO2����
��4��Al��������������Һ��Ӧ����Mg���ܣ���NaOH��Һ��ȥþ���л����������ۣ���Ӧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2����
�ʴ�Ϊ��NaOH��Һ��2Al+2NaOH+2H2O=2NaAlO2+3H2����
���� ���⿼�����ʵ������㡢һ�����ʵ���Ũ����Һ���ơ�Ԫ�ػ��������ʵȣ�ע��Ի���֪ʶ���������գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ���ʵ���Ũ�ȵ�������Һ��pH��a=b��c | |
| B�� | ͬpHʱ��������Һϡ����ͬ������pH��a=b��c | |
| C�� | ͬpH��ͬ�����������Һ����ͬŨ������������a=b=c | |
| D�� | ͬpHʱ��ϡ�Ͳ�ͬ������pH����ͬ��������Һϡ�͵ı�����a��b��c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ÿ����1 mol C3H8���������·�ṩ12 mol e- | |
| B�� | ����ͨ��C3H8��������ԭ��Ӧ | |
| C�� | ����ͨ��������CO2��������Ӧʽ�ǣ�O2+2CO2+4e-�T2CO32- | |
| D�� | CO32-�����ص����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���顢��ȩ�����ᶼ������ͬ���칹�壬����ѣ�CH3OCH3��Ҳ��ͬ���칹�� | |
| B�� | ���ۡ���֬�������ʡ���ά�ض�����������ˮ�⣬Ҳ�������������ṩ���� | |
| C�� | 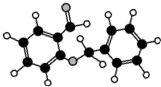 ��ͼ��ʾ���л������ʽΪC14H12O2���ܷ���������Ӧ | |
| D�� | �ڼ��������£�CH3CO18OC2H5��ˮ�������CH3COOH��C2H518OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ���ȡ�H=-890.3kJ/mol�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3 kJ/mol | |
| B�� | һ�������£���0.5 mol N2��1.5 molH2�����ܱ������г�ַ�Ӧ����NH3����19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-38.6 kJ/mol | |
| C�� | ��101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+O2��g���T2H2O��l����H=-571.6 kJ/mol | |
| D�� | HCl��NaOH��Ӧ���к��ȡ�H=-57.3 kJ/mol����H2SO4��Ba��OH��2��Ӧ���к��ȡ�H=2����-57.3��kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��pH=12����Һ�У�K+��Cl-��HCO3-��Na+ | |
| B�� | ��[H+]=10-12 mol•L-1����Һ��K+��Ba2+��Cl-��Br- | |
| C�� | ʹ��̪��Һ������Һ��Na+��Cl-��SO42-��Fe3+ | |
| D�� | ʹʯ����Һ������Һ��K+��MnO4-��I-��H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+ Na+CO32- Cl- | B�� | Mg2+ Na+Cl- SO42- | ||
| C�� | K+ NH4+ SO42-OH- | D�� | Fe2+ Al3+ NO3-H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
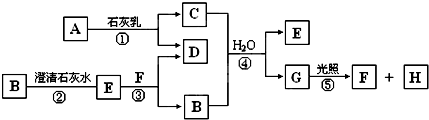
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
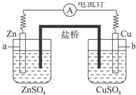
| A�� | �������Ų�Ӱ���ԭ��صĹ��� | |
| B�� | ��ع���ʱ��������K+����Zn�缫һ���ƶ� | |
| C�� | ��ع���ʱ��������Cl-����Zn�缫һ���ƶ� | |
| D�� | ��ع���ʱ�������еĵ�����Cu�缫��Zn�缫�ƶ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com