


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、6.72L CO |
| B、0.1NA CO2 |
| C、8 g SO3 |
| D、9.6g H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
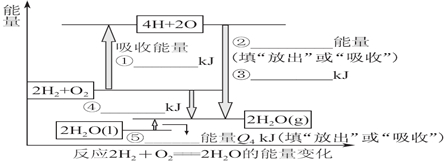
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一.
化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一.查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 | 结论 | |
| ① | 取少量上述漂白粉于试管中,加入适量1mol/L盐酸溶解后,再将产生的气体导入到澄清石灰水中 | 石灰水变浑浊 | |
| ② | 向上述反应后的试管滴入1~2滴品红溶液,振荡 | 品红褪色 | |
| 实验内容 | 将氯气持续通入淀粉碘化钾溶液 |
| 实验现象 | 溶液先变蓝,后褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、.+5价 |
| B、+4价 |
| C、+3 价 |
| D、+2 价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增加碳的量 |
| B、将容器体积缩小一半 |
| C、保持温度和体积不变,充入氖气 |
| D、保持温度和压强不变,充入氖气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com