
【题目】设![]() 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是 ![]()
![]()
A.![]() 的
的![]() 中含有的质子数与中子数均为
中含有的质子数与中子数均为![]()
B.![]() 的
的![]() 的核内中子数为N,质量数为
的核内中子数为N,质量数为![]() 的核外电子数为
的核外电子数为![]()
C.![]() 与
与![]() 混合气体中含
混合气体中含![]() 键的数目为
键的数目为![]()
D.![]() 和
和![]() 的固体混合物中含有的阳离子数为
的固体混合物中含有的阳离子数为![]()
【答案】CD
【解析】
A.1个![]() H
H![]() O中含有10个中子和10个质子,则10g
O中含有10个中子和10个质子,则10g ![]() 的物质的量n=
的物质的量n=![]() =
=![]()
![]() ,0.5mol
,0.5mol![]() ,含有的质子数与中子数均为5N
,含有的质子数与中子数均为5N![]() ,故A正确;
,故A正确;
B.阳离子的质子数比电子数多,则amol的![]() 的核外电子数为
的核外电子数为![]() NA,故B正确;
NA,故B正确;
C.26gC2H2中含有C—H键物质的量为![]() ×2=2mol,26gC2H6中含有C—H键物质的量为
×2=2mol,26gC2H6中含有C—H键物质的量为![]() ×6=5.2mol,26gC2H2与C2H6的混合气中含C—H键物质的量介于2mol~5.2mol之间,故C错误;
×6=5.2mol,26gC2H2与C2H6的混合气中含C—H键物质的量介于2mol~5.2mol之间,故C错误;
D.NaHSO4和KHSO3的摩尔质量都是120g/mol,则120gNaHSO4和KHSO![]() 的固体混合物的物质的量n=
的固体混合物的物质的量n=![]() =
=![]() =1mol,1molNaHSO4固体和1molKHSO3固体中都含1mol阳离子,则混合物中阳离子数N A,故D错误;
=1mol,1molNaHSO4固体和1molKHSO3固体中都含1mol阳离子,则混合物中阳离子数N A,故D错误;
答案选CD。


科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2A(g)+B(g)![]() 3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
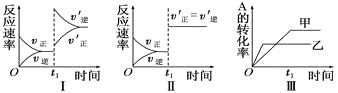
A. 图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响
B. 图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响
C. 图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
D. 图Ⅲ表示的是不同催化剂对平衡的影响,且甲的催化效率比乙高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 红棕色的NO2加压后颜色先变深后变浅 B. 温度过高对合成氨不利
C. 钢铁在潮湿的空气中容易生锈 D. 常温下,将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是实验室制取Cl2并以Cl2为原料进行特定反应的实验:

(1)A为氯气发生装置,写出反应的化学方程式_____________________.
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯.Cl2通入C瓶后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(气),试写出D装置中反应的化学方程式_______________.装置C的作用是________________.
(3)E处石蕊试液的现象是_____________,其原因是________________.
(4)若将E处溶液改为澄清石灰水,反应过程的现象是___________.
A.有白色沉淀生成 B.无白色沉淀生成
C.先生成白色沉淀,然后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是________________________________________.B的作用是___________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素,原子序数依次增大,A、E同主族,D、F同主族,A元素的原子半径是所有原子中最小的,B元素原子的最外层电子数是内层电子数的2倍,C元素的最高价氧化物的水化物X与其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
(1)F元素在周期表中的位置__________,在以上元素最高价氧化物的水化物中,碱性最强的化合物的电子式是:__________。
(2)D、F的气态氢化物,沸点较高的是___________(填分子式)。
(3)A单质与C单质在一定条件下可化合为Z,常温下,向pH=a的Z的水溶液中加入等体积pH=b的X的水溶液,且a+b=14,充分作用后,溶液pH______7(填“>”“<”或“=”),原因是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 1 mol SiO2晶体中,含有 SiO键的数目为2 NA
B. 16.8 g铁粉与足量高温水蒸气反应,转移电子数为0.8 NA
C. 1 mol·L1AlCl3溶液中,含有Cl的数目为3 NA
D. 18 g D2O和H2O的混合物中,含有的中子数为9 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向二元弱酸H2Y溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示。下列有关说法正确的是
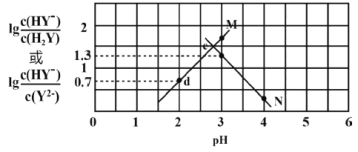
A.曲线N表示pH与![]() 的变化关系
的变化关系
B.交点e的溶液中:c(H2Y)=c(Y2-)>c(HY-)>c(H+)>c(OH-)
C.d点溶液中:c(H+)-c(OH-)=c(Y2-)+c(HY-)-c(K+)
D.Ka2(H2Y)=10-4.3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】几种物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含少量的FeCl3,为制得纯净CuCl2溶液,宜加入___________调至溶液pH=4,使Fe3+转化为Fe(OH) 3沉淀,此时溶液中的c(Fe3+)=_____________。
(2)过滤后,将所得滤液经过________,________操作,可得到CuCl2·2H2O晶体。
(3)由CuCl2·2H2O晶体得到纯的无水CuCl2,需要进行的操作是________________。
(4)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.800 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。过滤后,滤液用0.1000 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液40.00 mL。(已知:I2+2S2O32-=S4O32-+2I-)。
①可选用________作滴定指示剂,滴定终点的现象是__________________________。
②CuCl2溶液与KI反应的离子方程式为________________________________。
③该试样中CuCl2·2H2O的质量百分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学一有机化学基础](13分)
对二甲苯(英文名称p-xylene,缩写为PX)是化学工业的重要原料。
(1)写出PX的结构简式 。
(2)PX 可发生的反应有 、 (填反应类型)。
(3)增塑剂(DEHP)存在如下图所示的转化关系,其中A 是PX的一种同分异构体。
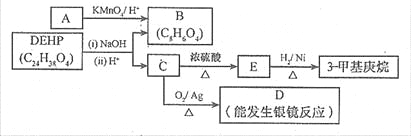
① B 的苯环上存在2 种不同化学环境的氢原子,则B 的结构简式是 。
② D 分子所含官能团是 (填名称)。
③ C 分子有1个碳原子连接乙基和正丁基,DEHP的结构简式是
(4)F 是B 的一种同分异构体,具有如下特征:
a.是苯的邻位二取代物;b.遇FeCl3溶液显示特征颜色;c.能与碳酸氢钠溶液反应。
写出F 与NaHCO3溶液反应的化学方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com