
【题目】黄钾铵铁矾[KNH4Fex(SO4)y(OH)z]不溶于水和稀硫酸,制取黄钾铵铁矾的示意图如下:

(1)溶液X是 。
(2)检验滤液中是否存在K+的操作是 。
(3)黄钾铵铁矾的化学式可通过下列实验测定:
① 称取一定质量的样品加入稀硝酸充分溶解,将所得溶液转移至容量瓶并配制成100.00 mL溶液A。
② 量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体9.32 g。
③ 量取25.00 mL溶液A,加入足量NaOH溶液,加热,收集到标准状况下气体224 mL,同时有红褐色沉淀生成。
④ 将步骤③所得沉淀过滤、洗涤、灼烧,最终得固体4.80 g。
通过计算确定黄钾铵铁矾的化学式(写出计算过程)。
【答案】(1)氨水(或NH3·H2O)
(2)用洁净的铂丝(或铁丝)蘸取滤液在酒精灯火焰上灼烧,透过蓝色钴玻璃观察,若火焰呈紫色,则存在K+(没有答到透过蓝色钴玻璃观察,不给分)
(3)n(SO![]() )= n(BaSO4)=
)= n(BaSO4)=![]() =0.04mol
=0.04mol
n(NH![]() )= n(NH3)=
)= n(NH3)=![]() =0.01mol
=0.01mol
n(Fe3+)=2 n(Fe2O3)=2×![]() =0.06mol
=0.06mol
n(K+)= n(NH![]() )=0.01mol
)=0.01mol
根据电荷守恒:n(OH-)= n(K+)+ n(NH![]() )+ 3n(Fe3+)-2 n(SO
)+ 3n(Fe3+)-2 n(SO![]() )=0.12mol
)=0.12mol
n(K+):n(NH![]() ):n(Fe3+): n(SO
):n(Fe3+): n(SO![]() ) :n(OH-)=1:1:6:4:12
) :n(OH-)=1:1:6:4:12
黄钾铵铁矾的化学式为KNH4Fe6(SO4)4(OH)12
【解析】
试题分析:(1)制取黄钾铵铁矾的示意图及黄钾铵铁矾[KNH4Fex(SO4)y(OH)z]组成,可以可知加入X是氨水,以便生成黄钾铵铁矾;
(2)通过焰色反应检验钾离子存在情况,方法为:用洁净的铂丝(或铁丝)蘸取滤液在酒精灯火焰上灼烧,透过蓝色的钴玻璃观察,若火焰呈紫色,则存在K+,
故答案为:用洁净的铂丝(或铁丝)蘸取滤液在酒精灯火焰上灼烧,透过蓝色的钴玻璃观察,若火焰呈紫色,则存在K+;
(3)②的沉淀为硫酸钡,硫酸钡的物质的量就等于溶液中硫酸根的物质的量:n(SO42-)=n(BaSO4)=![]() =0.04 mol
=0.04 mol
③所得气体为氨气,溶液中铵离子物质的量就等于氨气的物质的量:n(NH4+)=n(NH3)=![]() =0.01 mol
=0.01 mol
④最终得到的固体是氧化铁,根据铁原子守恒,溶液中的铁离子物质的量为:n(Fe3+)=2n(Fe2O3)=2×![]() =0.06 mol
=0.06 mol
黄钾铵铁矾[KNH4Fex(SO4)y(OH)z]中,n(K+)=n(NH4+)=0.01 mol,
根据电荷守恒:n(OH-)=n(K+)+n(NH4+)+3n(Fe3+)-2n(SO42-)=0.12 mol
n(K+):n(NH4+):n(Fe3+):n(SO42-):n(OH-)=1:1:6:4:12
黄钾铵铁矾的化学式为KNH4Fe6(SO4)4(OH)12,。


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
【题目】在相同温度和压强下,对反应CO2(g)+H2O(g)![]() CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内的各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内的各组分的物质的量见下表
物质 物质的量 实验 | CO2 | H2 | CO | H2O |
甲 | a mol | a mol | 0mol | 0mol |
乙 | 2a mol | a mol | 0mol | 0mol |
丙 | 0mol | 0mol | a mol | a mol |
丁 | a mol | 0mol | a mol | a mol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A.乙=丁>丙=甲 B.乙>丁>甲>丙 C.丁>乙>丙=甲 D.丁>丙>乙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如图所示。

请回答下列问题:
(1)A的结构简式为 ,B分子中的官能团名称为 。
(2)反应⑦中物质X的分子式为 ,反应⑧的类型为 。
(3)反应⑤的化学方程式为 。
反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是 。
(4)已知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的分子式为 。
(5)请补充完整证明反应①是否反应完全的实验方案: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据《天工开物》记载,我国古代以炉甘石(主要成分是ZnCO3)来冶炼倭铅(即锌),其原理如图2。已知锌的熔点420℃、沸点906℃。则下列说法错误的是( )

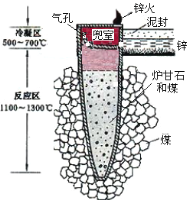
图1 图2
A.“泥封”的目的是为了防止得到的锌被氧化
B.“锌火”是锌蒸气和一氧化碳在空气的燃烧
C.冶炼时锌变为蒸气在兜室冷凝为固体
D.升炼倭铅过程包含分解反应和氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明同学在化学兴趣小组中提出一个猜想:“根据学习过的化学反应CaCO3+CO2+H2O=Ca(HCO3)2可以知道,Na2CO3溶液也能与CO2发生反应”。
为了确定小明同学猜想是否正确,兴趣小组在老师的指导下,通过实验探究的方法,完成了对该猜想的判。请你完成兴趣小组在实验探究活动中的部分实验报告。
【实验目的】:探究Na2CO3溶液与CO2的反应
【实验药品】:Na2CO3溶液、饱和的NaHCO3溶液、大理石、CaCl2、CaO、稀盐酸、稀硫酸、浓硫酸、澄清石灰水
【查阅资料】:NaHCO3与Ca(OH)2发生反应:2NaHCO3+ Ca(OH)2=CaCO3↓+Na2CO3+2H2O,碳酸氢钠与氯化钙溶液反应生成碳酸钙沉淀、氯化钠、水和二氧化碳。
【实验装置】;

【实验操作步骤与现象】
①写出实验室制取二氧化碳的化学方程式__________________。
②将制取的CO2通过饱和的NaHCO3溶液洗气瓶的目的是_____________。
③使过量的CO2通过装置Ⅲ,充分反应后,将其中所得的溶液取出3mL于试管中,然后向试管中加入______试剂(请从以上给出的药品中选择)当试管中出现_______现象时,Na2CO3溶液与CO2发生了化学反应,其反应的化学方程式为____________________________________。
【结论】:通过实验探究,小明同学的猜想是正确的。
【应用】:你能否依据此化学反应的规律,再写出一个类似的化学反应方程式(写上述已有的两个反应
不得分):________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。

(1)氯化炉中Al2O3、Cl2和C反应的化学方程式为 。
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式为 。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是 。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32 g。
①写出上述除杂过程中涉及的离子方程式:
②AlCl3产品的纯度为
(5)工业上另一种以铝灰为原料制备无水AlCl3的工艺中,最后一步是由AlCl3·6H2O脱水制备无水AlCl3,实现这一步的方法是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:
(1)Tl3++2Ag=Tl++2Ag+
(2)Ag++Fe2+=Ag+Fe3+
(3)Fe+2Fe3+=3Fe2+,
下列离子氧化性比较顺序正确的是( )
A.Tl3+>Fe3+>Ag+ B.Fe3+>Ag+>Tl3+
C.Tl+>Ag+>Fe2+ D.Tl3+>Ag+>Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列六种物质中:①乙醛②乳酸( )③乙烯④葡萄糖⑤乙醇
)③乙烯④葡萄糖⑤乙醇
(1)能发生酯化反应的是
(2)能发生银镜反应的是
(3)同种分子能通过加聚反应生成高分子化合物的是
(4)同种分子能通过缩聚反应生成高分子化合物是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com