
【题目】下列有关金属及其化合物的说法正确的是
A.铝和氢氧化钠溶液反应生成Al(OH)3和H2O
B.钠在空气中燃烧生成淡黄色的Na2O
C.铁在高温下与水蒸气反应生成Fe2O3和H2
D.碳酸钠溶液和氢氧化钙溶液反应生成NaOH和CaCO3
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是

A. 水合铜离子的模型如图1所示,1个水合铜离子中有4个配位键
B. CaF2晶体的晶胞如图2所示,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图3所示,H原子核外大多数电子在原子核附近运动
D. 金属Cu中Cu原子堆积模型如图4,为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应方程式正确的是( )
A. 苯酚与纯碱溶液混合反应的离子方程式:2C6H5OH + CO32-→CO2↑+ H2O + 2C6H5O-
B. 溴乙烷与氢氧化钠水溶液反应:![]()
C. 醋酸除水垢的离子方程式:CaCO3 + 2H+= Ca2+ + CO2↑+H2O
D. 苯甲醇与氧气发生催化氧化:2C6H5CH2OH + O2![]() 2C6H5CHO + 2H2O
2C6H5CHO + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钠用作甲状腺肿瘤防治剂、祛痰剂和利尿剂等。实验室用NaOH、单质碘和水合肼(N2H4·H2O)为原料可制备碘化钠。
资料显示:水合肼有还原性,能消除水中溶解的氧气;NaIO3是一种氧化剂。
回答下列问题:
(1)水合肼的制备:有关反应原理为:NaClO + 2NH3 = N2H4·H2O + NaCl。
①用下图装置制取水合肼,其连接顺序为_________(按气流方向,用小写字母表示)。
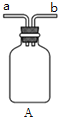
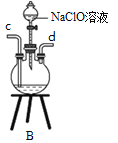
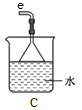
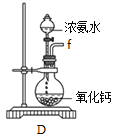
②装置A的作用是_______。
③开始实验时,先向氧化钙中滴加浓氨水,一段时间后再向B的三口烧瓶中滴加NaClO溶液。滴加NaClO溶液时不能过快的理由___________。
(2)碘化钠的制备
ⅰ.向三口烧瓶中加入8.4gNaOH及30mL水,搅拌、冷却,加入25.4g碘单质,开动磁力搅拌器,保持60~70℃至反应充分;
ⅱ.继续加入稍过量的N2H4·H2O(水合肼),还原NaIO和NaIO3,得NaI溶液粗品,同时释放一种空气中的气体;
ⅲ.向上述反应液中加入1.0g活性炭,煮沸半小时,然后将溶液与活性炭分离;
ⅳ.将步骤ⅲ分离出的溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得产品24.0g。
④步骤ⅰ适宜采用的加热方法是水浴加热, 该步骤反应完全的现象是_________。步骤ⅱ中IO3-参与反应的离子方程式为________________________________。
⑤步骤ⅲ “将溶液与活性炭分离”的方法是趁热过滤。
⑥本次实验产率为__________。实验发现,水合肼实际用量比理论值偏高,可能的原因是___________。
⑦某同学检验产品NaI中是否混有NaIO3杂质。取少量固体样品于试管中,加水溶解,滴加少量淀粉液后再滴加适量稀硫酸,片刻后溶液变蓝。得出NaI中含有NaIO3杂质。请评价该实验结论的合理性____________。(若认为合理写出离子方程式,若认为不合理说明理由)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质的有关叙述中正确的是( )
A. 乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色
B. 乙酸与乙醇可以发生酯化反应,又均可与金属钠发生置换反应
C. 分馏、干馏都是物理变化,裂化、裂解都是化学变化
D. 纤维素![]() 葡萄糖
葡萄糖![]() CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢(H2O2)溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。H2O2能与SO2反应生成H2SO4, H2O2的分子结构如图所示。下列说法错误的是( )
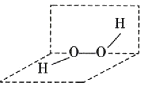
A. H2O2的结构式为H—O—O—H
B. H2O2为含有极性键和非极性键的共价化合物
C. 与SO2在水溶液中反应的离子方程式为SO2+ H2O2=2H++SO42-
D. H2O2与SO2反应过程中有共价键断裂,同时有共价键和离子键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小粒金属钠投入到盛有冷水的小烧杯中,以下描述合理的是
A. 无明显现象 B. 烧杯内溶液颜色逐渐变红
C. 金属钠浮于液面上,四处游动 D. 金属钠沉入烧杯底部,并产生气泡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛被称为继铁、铝之后的第三金属,其单质及化合物在航天、军事、航海、医疔等领域都有着重要的应用。请回答下列问题:
(1)基态Ti原子的价电子轨道表示式为___________。
(2)化学式为[Ti(H2O)6]Cl3的绿色晶体是TiCl3的六水合物的一种晶型,该晶体中,与Ti3+形成配位键的原子是___________ (填元素符号),该原子的杂化类型为___________杂化,该晶体所含元素中,电负性最大的元素是___________ (填元素符号)。
(3)化学式为[Ti(H2O)5 Cl]Cl2·H2O的绿色晶体是TiCl3的六水合物的另一种晶型,取1mol该晶体溶于水配成500mL溶液,加入足量AgNO3溶液使Cl-完全沉淀,消耗AgNO3的物质的量为___________mol。
(4)钛与卤素形成的化合物的熔沸点如下表所示,
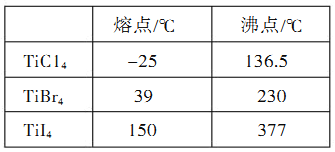
TiCl4、TiBr4、TiI4的熔点和沸点呈现一定变化规律的原因是______________________。
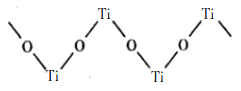
(5)TiO2能溶浓硫酸并析出一种离子晶体,已知其中阳离子是以链状聚合物形式存在的钛酰阳离子,其结构如下图所示,阳离子化学式为___________,写出一种与SO42-互为等电子体的分子___________。
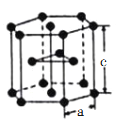
(6)下图是钛晶体在空间的一种堆积方式,此堆积方式名称为___________,钛原子的配位数为__________。已知:a=0.295nm,c=0.469nm,则该钛晶体的密度为___________g·cm-3(NA表示阿伏加德罗常数的值,列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com