
| A、若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| B、由水溶液的酸性:HCI>H2S,可推断出元素的非金属性:CI>S |
| C、邻羟基苯甲醛沸点高于对羟基苯甲醛是因为形成了分子内氢键 |
| D、H-F、H-O、H-N三种共价键的极性逐渐增强 |


科目:高中化学 来源: 题型:
| A、Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 | ||
| B、常温下,1 mol?L-1的CH3COOH溶液与1 mol?L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | ||
| C、常温下,某溶液中由水电离出的c(H+)=10-5mol?L-1,则此溶液可能是盐酸 | ||
D、物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应的热效应与反应途径无关 |
| B、化学反应的热效应与反应的起始状态和最终状态有关 |
| C、应用盖斯定律,可计算某些难以直接测量热效应的反应 |
| D、盖斯定律只适用于化学反应的能量变化,不适用于物质聚集状态转化时能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2H2(g)+O2(g)=2H2O(g),△H 1; 2H2(g)+O2(g)=2H2O(l),△H2 | ||||
| B、S(g)+O2(g)=SO2(g),△H1; S(s)+O2(g)=SO2(g),△H2 | ||||
C、C(s)+
| ||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、②③⑥ |
| C、⑤⑥ | D、④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
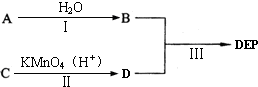 北京市疾病预防控制中心的调查结果显示,在北京市场上有九成受检香水和三成护发类化妆品被查出致癌物“邻苯二甲酸酯”(PAEs),值得注意的是,在儿童护肤类化妆品中亦有两件样品分别被检出邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二(2-乙基己基)酯(DEHP).
北京市疾病预防控制中心的调查结果显示,在北京市场上有九成受检香水和三成护发类化妆品被查出致癌物“邻苯二甲酸酯”(PAEs),值得注意的是,在儿童护肤类化妆品中亦有两件样品分别被检出邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二(2-乙基己基)酯(DEHP).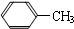
| KMnO4(H+) |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com