
| A. | 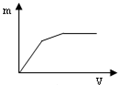 | B. |  | C. | 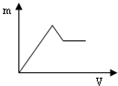 | D. | 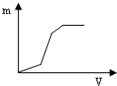 |
分析 4mol HCl和1mol MgSO4的混合溶液中含有4mol氢离子、1mol镁离子和1mol硫酸根离子,混合液中滴入Ba(OH)2溶液后,氢离子、钡离子优先反应,只有氢离子反应完全后镁离子才与氢氧根离子反应生成氢氧化镁沉淀,所以开始时只生成硫酸钡沉淀;当加入1molBa(OH)2后,硫酸根离子反应完全,氢离子还剩余2mol,此时再滴入Ba(OH)2溶液,只有氢离子参与反应,则沉淀的量暂时不变;当加入的Ba(OH)2为2mol时,氢离子反应完全,此后镁离子开始与氢氧根离子反应,所以沉淀的量开始增加,之至镁离子完全沉淀、沉淀量达到最大,反应停止,据此进行解答.
解答 解:4mol HCl和1mol MgSO4的混合溶液中含有4molH+、1molMg2+和1molSO42-,
混合液中滴入Ba(OH)2溶液后,H+、Ba2+优先反应,只有H+反应完全后Mg2+才开始与氢氧根离子反应生成氢氧化镁沉淀,所以开始时只生成BaSO4沉淀;
当加入1molBa(OH)2后,SO42-反应完全,H+还剩2mol,此时再滴入Ba(OH)2溶液,只有H+参与反应,则沉淀的量暂时不变;
当加入的Ba(OH)2为2mol时,H+反应完全,此后Mg2+开始与OH-反应Mg2++2OH-═Mg(OH)2↓,所以沉淀的量又开始增加,直至Mg2+完全沉淀、沉淀量达到最大,
根据分析画出产生的沉淀质量m与加入Ba(OH)2溶液体积V的图象为: ,
,
故选B.
点评 本题考查了混合物反应的计算及应用,题目难度不大,明确发生反应的原理及先后顺序为解答关键,试题侧重考查学生的分析、理解能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题
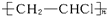 .
.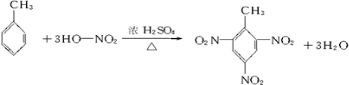 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
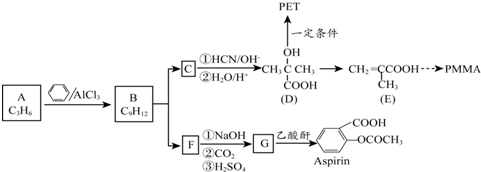
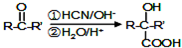
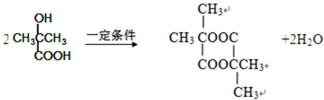 .1mol Aspirin分子与足量的NaOH反应的化学方程式是
.1mol Aspirin分子与足量的NaOH反应的化学方程式是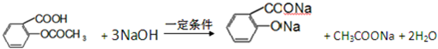 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
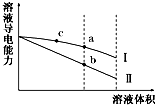 常温下,将一定浓度的盐酸和醋酸加水稀释,溶液的导电能力随溶液体积变化的曲线如图所示.判断下列说法中,正确的是( )
常温下,将一定浓度的盐酸和醋酸加水稀释,溶液的导电能力随溶液体积变化的曲线如图所示.判断下列说法中,正确的是( )| A. | 两溶液稀释前的浓度相同 | |
| B. | a、b、c三点溶液的pH由大到小顺序为a>b>c | |
| C. | a点的KW值比b点的KW值大 | |
| D. | a点水电离的c(H+)大于c点水电离的c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水、二氧化硫、活性炭的漂白或脱色原理虽然不同,但它们都能使品红或墨迹褪色 | |
| B. | 等物质的量的Cl2和SO2同时与潮湿的红布条作用,红布条立即褪色 | |
| C. | 反应CuSO4+H2S=CuS↓+H2SO4能进行,说明硫化铜既不溶于水,也不溶于稀硫酸 | |
| D. | 经Cl2和SO2漂白的物质,日后都会恢复原来的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①③⑥ | C. | ①②③ | D. | ②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com