
对处于平衡状态的反应2A(g)+B(g) 2C(g) △H<0,下
2C(g) △H<0,下
列叙述正确的是
A.增大A浓度的瞬间,V正 增大,V逆不变 B.升高温度,V正 减小,V逆增大
C.增大压强. V正 增大,V逆 减小 D.加入催化剂,V正、V逆 都增大
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
钾水玻璃以其优异的性能广泛用于防腐、铸造、油田、钻井或各种高档涂料中。钾水玻璃中硅含量的测定可以采用氟硅酸钾容量法,其步骤为:
①称取试样溶解在含有过量的氟离子和钾离子的强酸溶液中,硅能与氟离子、钾离子作用生成氟硅酸钾(K2SiF6)沉淀;
②沉淀分离后于热水中水解,生成HF、H2SiO3、KF;
③过滤除去硅酸沉淀,用氢氧化钠标准溶液滴定滤液。
(1)上述步骤②中的水解反应方程式为 ▲ ;
步骤③中反应的离子方程式为: ▲ 。
(2)在步骤③中,若滴定前未用氢氧化钠标准溶液润洗滴定管,则测得的硅元素含量将
▲ (填“偏高”、或“偏低”或“不变”)。
(3)若每次称取试样的质量为1.00g,重复滴定四次,消耗1.00 mol·L-1氢氧化钠标准溶液的体积为分别为16.80mL、19.90mL、20.00mL、20.10mL,试计算该试样中硅元素的质量分数(以二氧化硅计),写出计算过程。 ▲
查看答案和解析>>
科目:高中化学 来源: 题型:
古时候有一个勇敢的小伙子想娶国王女儿——美丽的公主,国王出题刁难,其中的一个问题是:10 kg小米是多少粒?小伙子很快就想到了解决这个问题的办法,顺利地娶到了公主,你能不能想到小伙子想到了什么方法?______________________________________。
借助这种方法,我们也可以设置一个物理量,假定一定量的物质有多少个微粒,那么我们就能很好地将宏观物质和微观物质联系起来。这个物理量是________________,它的基准是________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
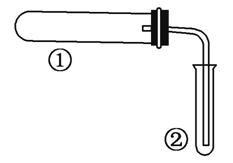
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是( )
| 选项①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于化学反应限度的叙述,错误的是( )
A.任何可逆反应都有一定的限度
B.化学反应达到限度时,正、逆反应速率相等
C.化学反应的限度与时间的长短无关
D.化学反应的限度是不可改变的
查看答案和解析>>
科目:高中化学 来源: 题型:
在373 K时,密闭容器中充入一定量的NO2和SO2,发生如下反应:NO2+SO2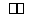 NO+SO3,平衡时,下列叙述正确的是( )
NO+SO3,平衡时,下列叙述正确的是( )
①NO和SO3的物质的量一定相等 ②NO2和SO2的物质的量一定相等 ③体系中的总物质的量一定等于反应开始时总物质的量 ④SO2、NO2、NO、SO3的物质的量一定相等
A.①和 ② B.②和③
② B.②和③
C.①和③ D.③和④
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应mA(g) + nB(g)  pC(g) + qD(g),
pC(g) + qD(g),
若其它条件都不变,探究催化剂对反应的影响,可得到如下两种v-t图象。下列判断正确的是( )

A.b1>b2 ,t1>t2
B.两图中阴影部分面积一定相等
C.A的平衡转化率(II)大于(Ⅰ)中A的转化率
D.若m+n<p+q,则压强变化对正反应速率的影响程度比逆反应速率影响程度大
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应:H2(g)+I2(g)  2HI(g),在温度T1和T2时,产物的量与反应时间的关系如右图所示,符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如右图所示,符合图示的正确判断是
A.T1>T2,ΔH>0 B.T1>T2,ΔH<0
C.T1<T2,ΔH>0 D.T1<T2,ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2 L的 密闭容器中,保持体系内温度800 ℃不变,将一定量的NO和O2混合发生反应:
密闭容器中,保持体系内温度800 ℃不变,将一定量的NO和O2混合发生反应:
2NO+O22NO2,其中NO的物质的量(n)随时间(t)的变化关系如图所示。请回答下列问题。
(1)30 s时反应达到平衡,用O2表示达到平衡过程的平均反应速率为
________,图像中曲线______ __(选填“Ⅰ”或“Ⅱ”)表示NO2的变化。由图像中曲线和数据变化,能否计算该温度下的平衡常数:____________(填“能”或“不能”)。
__(选填“Ⅰ”或“Ⅱ”)表示NO2的变化。由图像中曲线和数据变化,能否计算该温度下的平衡常数:____________(填“能”或“不能”)。
(2)若升高反应体系的温度,使反应重新达到平衡,此时体系中n(NO)=n(NO2),则该反应是________热反应(选填“吸”或“放”)。
(3)在800 ℃时,若缩小容器的体积,达新平衡时n(NO)________(选填“>”、“=”或“<”)0.07 mol,NO的转化率________(选填“增大”、“不变”或“减小”)。
(4)上述800 ℃时的反应达到平衡时测得放出热量a kJ。试写出在此条件下NO与氧气反应的热化学方程式________________________________________ __________________________。
__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com