
【题目】靠一组镍氢电池驱动,一台试运行的混合动力公交车两年内跑了10万公里。大功率镍氢动力电池及其管理模块,是国家“十五”863计划电动汽车重大专项中一项重要课题。我国镍氢电池居世界先进水平,我军潜艇将装备国产大功率镍氢动力电池。常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均为零),电池反应通常表示为LaNi5H6+ 6NiO(OH)![]() LaNi5+ 6Ni(OH)2。下列说法正确的是
LaNi5+ 6Ni(OH)2。下列说法正确的是
A.放电时储氢合金作正极B.充电时储氢合金作阳极
C.充电时阳极周围c(OH-)增大D.放电时负极反应:LaNi5H6+ 6OH-- 6e-= LaNi5+ 6H2O
【答案】D
【解析】
此电池放电时的反应为LaNi5H6+ 6NiO(OH)![]() LaNi5+ 6Ni(OH)2,正极反应为6NiOOH+6H2O+6e-=6Ni(OH)2+6OH-,负极反应为LaNi5H6+ 6OH-- 6e-=LaNi5+6H2O。由此可见储氢合金失电子,作原电池的负极。充电是放电的逆反应,据此解答。
LaNi5+ 6Ni(OH)2,正极反应为6NiOOH+6H2O+6e-=6Ni(OH)2+6OH-,负极反应为LaNi5H6+ 6OH-- 6e-=LaNi5+6H2O。由此可见储氢合金失电子,作原电池的负极。充电是放电的逆反应,据此解答。
A、放电时是原电池,依据总反应化学方程式可知,储氢合金做电池的负极,故A错误;
B、充电时,储氢合金得电子发生还原反应,作阴极,故B错误;
C、充电时为电解池,阳极电极反应为:6Ni(OH)2+6OH--6e-=6NiOOH+6H2O,氢氧根离子浓度减小,故C错误;
D、放电时,负极失电子发生氧化反应,电极反应为:LaNi5H6+ 6OH-- 6e-=LaNi5+6H2O,故D正确;
故选:D。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】将V1mL 1.0 mol·L-1盐酸溶液和V2mL未知浓度的氢氧化钠溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。
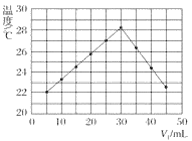
下列叙述正确的是( )
A.做该实验时环境温度为20 ℃
B.该实验表明化学能可能转化为热能
C.氢氧化钠溶液的浓度约为1.0 mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温州某学生用0.1000mol/L NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.用蒸馏水洗干净滴定管
B.用待测定的溶液润洗酸式滴定管
C.用酸式滴定管取稀盐酸20. 00mL,注入锥形瓶中,加入酚酞
D.另取锥形瓶,再重复操作一次
E.检查滴定管是否漏水
F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管“0”刻度以上2~3 cm处,再把碱式滴定管固定好,调节液面至“0”刻度或“0”刻度以下
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)______________。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察_____________________________。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
滴定终点溶液颜色的变化是__________________________________________。
(3)滴定结果如表所示:
滴定次数 | 待测液体积/mL | 标准溶液的体积/mL | ||
滴定前刻度 | 滴定后刻度 | |||
① | 20 | 1.02 | 21.03 | |
② | 20 | 2.00 | 25.00 | |
③ | 20 | 0.61 | 20.60 | |
滴定中误差较大的是第_______次实验,造成这种误差的可能原因是_______。
A.碱式滴定管在装液前未用标准NaOH溶液润洗2~3次
B.滴定开始前碱式滴定管尖嘴部分有气泡,在滴定终点读数时未发现气泡
C.滴定开始前碱式滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
D.达到滴定终点时,仰视溶液凹液面最低点读数
E.滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
(4)该盐酸的浓度为________mol/L。
(5)如果准确移取20. 00mL 0.1000mol/L NaOH溶液于锥形瓶中,滴入酚酞指示剂,然后用未知浓度的盐酸(装在酸式滴定管中)滴定,是否也可测定出盐酸的物质的量浓度?______________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是 ( )
CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是 ( )
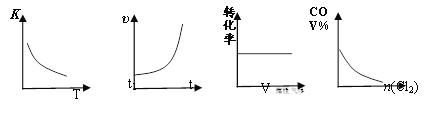
① ② ③ ④
A. ①表示随温度升高,平衡常数的变化
B. ②表示加入催化剂,反应速率随时间的变化
C. ③表示恒压条件下,反应物的转化率随充入惰性气体体积的变化
D. ④表示CO的体积分数随充入Cl2量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应CO2(g)+C(s)![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是

A.反应CO2(g)+C(s) ![]() 2CO(g)的ΔS>0、ΔH<0
2CO(g)的ΔS>0、ΔH<0
B.体系的总压强p总:p总(状态Ⅱ)<2p总(状态Ⅰ)
C.体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D.逆反应速率:v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.3kJ/moL,N2的平衡转化率a(N2)与体系总压强(p)的关系如图所示。下列说法正确的是( )
2NH3(g) ΔH=-92.3kJ/moL,N2的平衡转化率a(N2)与体系总压强(p)的关系如图所示。下列说法正确的是( )
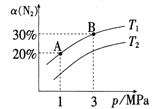
A.将1molN2与3molH2置于1L密闭容器中充分反应,放出的热量为92.3kJ
B.T1<T2
C.平衡状态由A变到B时,平衡常数K(A)<K(B)
D.升高温度,平衡向逆反应方向移动,逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁镍蓄电池又称爱迪生电池,放电时的总反应为![]() ,下列有关该电池的说法错误的是( )
,下列有关该电池的说法错误的是( )
A.电池的电解液为碱性溶液,正极为![]() 、负极为
、负极为![]()
B.电池放电时,正极反应为![]()
C.电池充电过程中,阴极附近溶液的![]() 升高
升高
D.电池充电时,阳极反应为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W的合成路线如图:
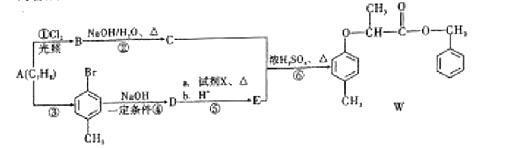
已知:ⅰ.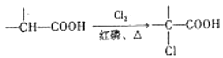 ;
;
ⅱ.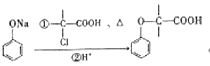 。
。
(1)W中的含氧官能团有醚键和__________,![]() 的反应类型为_____________。
的反应类型为_____________。
(2)D的名称为__________________。
(3)步骤⑥反应的化学方程式为_________________________________________________。
(4)试剂X的结构简式为_______________________。
(5)同时满足下列条件,E的同分异构体有__________种。(不考虑立体异构)
ⅰ.能与![]() 溶液发生显色反应;
溶液发生显色反应;
ⅱ.能发生水解反应和银镜反应;
ⅲ.苯环上只有两个取代基。
其中核磁共振氢谱峰面积比为1∶1∶2∶2∶6的分子的结构简式为_______________。
(6)根据以上信息,写出以![]() 为原料制取
为原料制取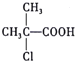 的合成路线图:_____________________________(无机试剂一定要选银氨溶液,其他无机试剂任选)
的合成路线图:_____________________________(无机试剂一定要选银氨溶液,其他无机试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g) ![]() C(g) +D(g) 发生过程中的能量变化如图,△H 表示反应的焓变。下列说法正确的是( )
C(g) +D(g) 发生过程中的能量变化如图,△H 表示反应的焓变。下列说法正确的是( )
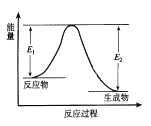
A. 反应体系中加入催化剂,反应速率增大,E1减小,E2增大
B. 反应体系中加入催化剂,反应速率增大,△H增大
C. △H < 0,反应达到平衡时,升高温度,A的转化率减少
D. △H > 0,反应达到平衡时,增大压强,A的转化率不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com