
分析 (1)根据用固体配制溶液的一般步骤为计算、称量、溶解转移、洗涤转移、定容摇匀,据此解答;
(2)根据配制一定物质的量浓度的溶液的具体操作步骤,选择所需的仪器,依据配置溶液的体积选择容量瓶的规格;
(3)分析操作对溶质的物质的量及溶液体积的影响,根据c=$\frac{n}{V}$判断误差.
解答 解:(1)用固体配制溶液的一般步骤为计算、称量、溶解、转移、洗涤、定容、摇匀、装瓶,
故答案为:计算;称量;溶解;转移;洗涤;定容;摇匀;
(2)配制1.00mol/L的NaCl溶液0.5L,应选择500mL容量瓶,称量需用药匙取氯化钠,溶解需要用烧杯,玻璃棒搅拌,转移过程中用玻璃棒引流,最后用胶头滴管定容,故还需要的玻璃仪器为:烧杯、玻璃棒、胶头滴管;
故答案为:500mL;烧杯、玻璃棒、胶头滴管;
(3)①为加速固体溶解,可稍微加热并不断搅拌,在未降至室温时,立即将溶液转移至容量瓶定容,溶液受热膨胀时体积为0.5 L,冷却至室温时体积变小,根据c=$\frac{n}{V}$可知,溶液浓度偏大;
故答案为:偏大;受热膨胀时体积为0.5 L,冷却至室温时溶液体积变小;
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,导致所溶液体积偏大,根据c=$\frac{n}{V}$可知,溶液浓度偏小;
故答案为:偏小;溶液体积增大,溶液体积增大,溶质的物质的量不变.
点评 本题考查一定物质的量浓度溶液的配制,难度不大,关键清楚溶液配制原理,注意根据c=$\frac{n}{V}$进行误差分析的方法.


科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④⑥ | C. | ①②③④ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
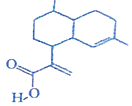
| A. | 该物质属于芳香族化合物 | B. | 该物质易溶于水 | ||
| C. | 能发生取代反应和加成反应 | D. | 分子中所有碳原子可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S的水解:S2ˉ+2H2O?H2S+2OHˉ | |
| B. | 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 硫酸亚铁酸性溶液中加入过氧化氢:2Fe2++H2O2+2H+=2Fe3++2H2O | |
| D. | 向NaClO溶液中通入少量SO2:2ClOˉ+SO2+H2O=SO32ˉ+2HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(mol•L-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶用蒸馏水洗净后,未待干燥便用来配制 | |
| B. | NaOH溶解后趁热移入容量瓶中 | |
| C. | 定容时,俯视刻度线 | |
| D. | 摇匀后发现液面未到刻度线,继续加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
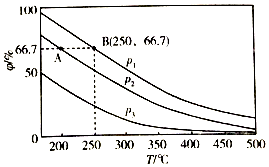 氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)?2NH3(g)△H.
氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)?2NH3(g)△H.| H-H | N-H | N-N | N |
| 435.9KJ | 390.8KJ | 192.8KJ | 945.8KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知五种短周期元素在周期表中的相对位置如表所示.
已知五种短周期元素在周期表中的相对位置如表所示.| a | |||||
| b | |||||
| c | d | e |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com