
 在密闭容器中进行如下反应:H2(g) +I2(g)
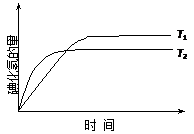
在密闭容器中进行如下反应:H2(g) +I2(g)![]() 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示,符合图示的正确判断是( )
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示,符合图示的正确判断是( )
A.T1>T2,ΔH>0 B.T1>T2,ΔH<0
C.T1<T2,ΔH>0 D.T1<T2,ΔH<0
D
根据“先拐先平”原则,先拐的到达平衡的时间短,对应的反应速率快,温度高。根据T2曲线先达到平衡说明T2高于T1,而T2时HI的含量低于T1时的含量,说明该反应为放热反应。显然D正确。
点评:借助图象考查化学平衡问题,是近年来备受高考青睐的一种命题形式。
解题的主要策略有:
①先根据“先拐先平”原则,判断出曲线对应的温度或压强的大小。“先拐先平”即先拐的说明达到平衡所需的时间短,对应的化学反应速率快,对应的温度或压强大。
②固定其中的一个因素(温度或压强),然后讨论另一个因素与化学平衡中的参量(百分含量、体积分数、平均相对分子质量)的变化关系,从而判断出该反应为放热反应或吸热反应、反应前后气体体积的大小关系。


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
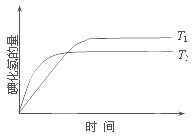 在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g);△H,在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )
在密闭容器中进行如下反应:H2(g)+I2(g)?2HI(g);△H,在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z为0.3 mol/L | B、Y为0.15 mol/L | C、X为0.1 mol/L | D、Z为0.4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
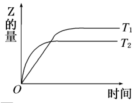
| A、T1<T2,正反应是放热反应 | B、T1<T2,正反应是吸热反应 | C、T1>T2,正反应是放热反应 | D、T1>T2,正反应是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com