

| A、CO、SO2、SO3均是酸性氧化物 |
| B、工业上利用Cl2和澄清石灰水反应来制取漂白粉 |
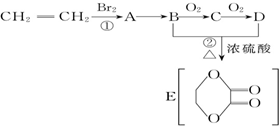
| C、除去与水反应,图3所示转化反应均为氧化还原反应 |
| D、用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100% |


科目:高中化学 来源: 题型:
| A、胶粒呵以导电 |
| B、它们是混合物 |
| C、胶体粒子大小在1~100nm之间 |
| D、分散剂为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、质量数为16的氧原子:
| ||||
| B、纯碱的化学式:NaHCO3 | ||||
C、Mg2+结构示意图: | ||||
D、铁丝在氯气中燃烧的化学方程式:Fe+Cl2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 “学生甲”通过中和滴定的方法,去测定在空气中露置一段时间后的NaOH固体的纯度,设计如下方案:
“学生甲”通过中和滴定的方法,去测定在空气中露置一段时间后的NaOH固体的纯度,设计如下方案:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要的时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | - |
| 3 | 900 | a | b | c | d | - |
| a |
| b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com