
A.H2(g) + I2(s) 2HI(g) - 26.5kJ 2HI(g) - 26.5kJ |
B.H2 + I2 2HI - 53kJ 2HI - 53kJ |
C.H2(g) + I2(s) 2HI(g) - 53kJ 2HI(g) - 53kJ |
D.0.5H2 + 0.5I2 HI - 26.5kJ HI - 26.5kJ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:问答题
 2NH3 (g) ΔH ="c" kJ? mol-1
2NH3 (g) ΔH ="c" kJ? mol-1

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g),SO2的平衡转化率与温度、压强的关系如右图所示。
2SO3(g),SO2的平衡转化率与温度、压强的关系如右图所示。
| 气体 | SO2 | O2 | SO3 |
| 浓度(mol/L) | 0.4 | 1.2 | 1.6 |
 。(已知该温度下H2SO3的电离常数:Ka1=1.0×10-2 mol/L,Ka2=6.0×10-3 mol/L)
。(已知该温度下H2SO3的电离常数:Ka1=1.0×10-2 mol/L,Ka2=6.0×10-3 mol/L)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2C(g)达到平衡时,各物质的
2C(g)达到平衡时,各物质的查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 (NH4)2CO3(aq) △H1
(NH4)2CO3(aq) △H1 (NH4)2HCO3(aq) △H2
(NH4)2HCO3(aq) △H2 2(NH4)2HCO3(aq) △H3
2(NH4)2HCO3(aq) △H3
| A.NH4Cl | B.Na2CO3 |
| C.HOCH2CH2OH | D.HOCH2CH2NH2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 O2(g)===CO(g) △H2
O2(g)===CO(g) △H2| A.①③ | B.①④ | C.②④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 )作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知
)作燃料,二氧化氮作氧化剂,两者反应生成氮气和气态水。已知 完全发生上述反应放出
完全发生上述反应放出 的热量,热化学方程式是:
的热量,热化学方程式是:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO+3H2的焓变△H=_______。
CO+3H2的焓变△H=_______。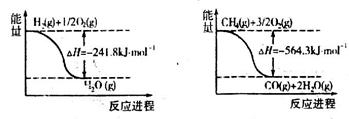
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com