
(Ⅰ)某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:
|
时间 H2O2 | 0.1 g | 0.3 g | 0.8 g |
| 10 mL 1.5% | 223 s | 67 s | 56 s |
| 10 mL 3.0% | 308 s | 109 s | 98 s |
| 10 mL 4.5% | 395 s | 149 s | 116 s |
请回答下列问题:
(1)盛装双氧水的化学仪器名称是 。
(2)如何检验该套装置的气密性 。
(3)相同浓度的过氧化氢,其分解速率随着二氧化锰用量的增加而________。
(4)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________g的二氧化锰为较佳选择。
(5)某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确________,理由是_______________________________________。(提示:H2O2的密度可认为近似相等)。
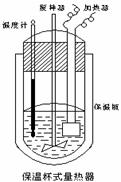 (Ⅱ)在如图所示的量热计中,将100mL 0.50mol·L-1CH3COOH溶
(Ⅱ)在如图所示的量热计中,将100mL 0.50mol·L-1CH3COOH溶
液与100mL0.55mol·L-1NaOH 溶液混合,温度从25.0℃升高到27.7℃。已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是
150.5J·℃-1生成溶液的比热容为4.184J·g-1·℃-1,溶液的密度均近似
为1g·mL-1。
(1)试求CH3COOH的中和热△H= 。
(2)CH3COOH的中和热的文献值为56.1KJ· mol-1,则请你分
析在(1)中测得的实验值偏差可能的原因 。
(3)实验中NaOH过量的目的是 。
【知识点】化学实验操作 F1 G2 G5
【答案解析】22、
(Ⅰ)(1)分液漏斗 1分
(2)关闭分液漏斗的活塞,将注射器的活栓向外拉出一段距离,若一段时间后活栓能够恢复到原位置,则装置的气密性好。 2分
(3)加快 1分
(4)0.3 1分
(5)不正确 1分
H2O2的浓度扩大二倍(从1.5%—→3.0%),但反应所需时间比其二倍小的多 2分
(Ⅱ)(6)—53.3kJ/mol 2分
(7)①量热计的保温瓶绝热效果不好;②酸碱溶液混合不迅速;③温度计不够精确等2分
(8)使碱稍稍过量,为了能保证CH3COOH溶液完全被中和,从而提高实验的准确度。2分
解析:I、(1)常考实验仪器,分液漏斗便于控制反应发生
(2)检验气密性为常考点,注意书写步骤
(3)根据表格横行可知,二氧化锰用量增加,分解速率加快
(4)选择0.3g二氧化锰,因为速率加快且催化剂量适量
(5)反应速率比较的是变化量,H2O2的浓度扩大二倍(从1.5%—→3.0%),但反应所需时间比其二倍小的多
II、:(1)CH3COOH的中和热Q=△H=Q=-cm△T=[150.5J·℃-1+4.184J·g-1·℃-1×1g·mL-1×200ml]×(27.7℃-25℃)/0.05mo=-53.3 kJ•mol-1
(2)实验值偏差可能是因为①量热计的保温瓶绝热效果不好;②酸碱溶液混合不迅速;③温度计不够精确等
(3) 酸和碱反应测中和热时,为了保证一方全部反应,往往需要另一试剂稍稍过量,减少实验误差
【思路点拨】本题考查学生中和热的测定知识,注意稀的强酸和强碱溶液发生中和反应生成1mol水所放出的热量即为中和热.


 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
下列化合物Ⅰ的说法,正确的是________。
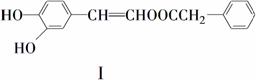
A.遇FeCl3溶液可能显紫色
B.可发生酯化反应和银镜反应
C.能与溴发生取代和加成反应
D.1 mol化合物Ⅰ最多能与2 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
我国首创以铝-空气-海水电池作为能源的新型海水标志灯,以海水为电解质,靠空气中的氧气使铝不断氧化而产生电流。只要把灯放入海水中数分钟,就会发出耀眼的白光。则该电源负极材料为________,正极材料为________,正、负极反应分别为________________________________________________________________________,
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
关于金属腐蚀的叙述中,正确的是( )
A.金属被腐蚀的本质是M+nH2O===M(OH)n+ H2↑
H2↑
B.马口铁(镀锡铁)镀层破损后被腐蚀时,首先是镀层被氧化
C.金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀
D.常温下,置于空气中的金属主要发生化学腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为________________________________________________________________________。
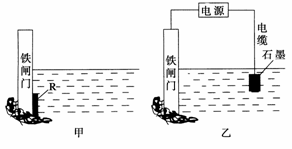
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用________(填字母)。
A.铜 B.钠 C.锌 D.石墨
(3)图乙所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的________极。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业合成氨与制备硝酸一般可连续生产,流程如图所示:
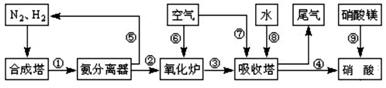
(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2
CO2+H2
T℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
(2)合成塔中发生反应N2(g)+3H2(g) 2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____573K(填“>”、“<”或“=”)。
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1____573K(填“>”、“<”或“=”)。
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
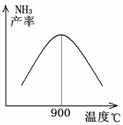
(3)N2和H2以铁作催化剂从145℃就开始反应,不同温度下NH3的产率如图所示。温度高于900℃时,NH3产率下降的原因是
(4)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2=(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:
(5)氨气在纯氧中燃烧,生成一种单质和水。科学家利用此原理,设计成氨气-氧气燃料电池,则通入氨气的电极碱性条件下发生反应的电极反应式为
。
查看答案和解析>>
科目:高中化学 来源: 题型:
同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是 ( )
A.2Na218O2 + 2H2O = 4Nal8OH + O2↑
B.NH4Cl + 2H2O  NH3·2H2O + HCl
NH3·2H2O + HCl
C.2KMnO4 + 5H218O2 + 3H2SO4= K2SO4 + 2MnSO4 + 518O2↑ + 8H2O
D.K37ClO3 + 6HCl = K37Cl + 3Cl2↑ + 3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
①电解质溶液导电属于化学变化
②碱性氧化物都是金属氧化物
③FeCl2、Fe(OH)3、Fe3O4都能通过化合反应来制取
④Na2O2不是碱性氧化物
A.②③④ B.①④
C.①②③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
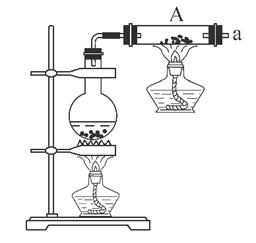
(1)铁粉与水蒸气反应的化学方程式是: ;
(2)为检验生成的气体产物,需从下图选择必要的装置,其正确的连接顺序为(用接口字母表示)a— ,描述能证明气体产物的实验现象_ ;
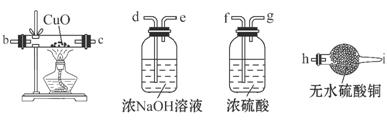
(3)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法: ;
(4)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是(用化学方程式说明): ;
(5)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是: ;
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有同学设计如下图所示的装置: 通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是________(填序号)。
通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是________(填序号)。
A.电源中的a为正极,b为负极 B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极 D.阴极发生的反应是2H++2e-===H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com