
| A. | 苯的最简式:C6H6 | B. | 乙烯分子的结构简式为:CH2CH2 | ||
| C. | 一氯甲烷的电子式为: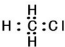 | D. | 2-甲基丁烷的键线式: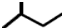 |
分析 A.最简式为分子中各原子数目的最简比,C6H6为分子式;
B.乙烯分子中含有碳碳双键,结构简式中没有标出碳碳双键;
C.一氯甲烷的电子式中没有标出氯原子的3对孤电子对;
D.2-甲基丁烷的主链为丁烷,甲基在2号C原子.
解答 解:A.苯的分子式为C6H6,则苯的最简式为CH,故A错误;
B.乙烯分子中含有1个碳碳双键,其正确的结构简式为:CH2=CH2,故B错误;
C.一氯甲烷中碳原子和氯原子最外层都达到8电子稳定结构,其正确的电子式为 ,故C错误;
,故C错误;
D.2-甲基丁烷中,主链为丁烷,在2号C上含有1个甲基,其键线式为: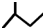 ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法判断,题目难度不大,涉及比例模型、电子式、结构简式、键线式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的分析能力及规范答题能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Na2CO3 NaHCO3 CH3COONa NaF | |
| B. | NaHCO3 Na2CO3 CH3COONa NaF | |
| C. | NaF CH3COONa Na2CO3 NaHCO3 | |
| D. | NaF CH3COONa NaHCO3Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnCl2溶液中常含有Cu2+,可添加难溶电解质MnS除去:Cu2++S2-=CuS↓ | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞是因为:SiO2+2OH-=SiO32-+H2O | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 向氨水中滴入少量饱和氯化铁溶液制各Fe(OH)3胶体:Fe3++3NH3•H2O?Fe(OH)3(胶体)+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6:3:2 | B. | 1:2:3 | C. | 3:6:2 | D. | 2:1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D2+>B2+>A2+>C2+ | B. | A2+>B2+>C2+>D2+ | C. | C2+>A2+>B2+>D2+ | D. | A2+>C2+>D2+>B2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
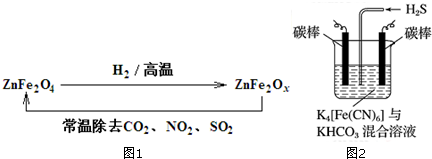
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热的反应发生时不必加热,吸热反应都需要加热后才能发生 | |
| B. | 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 | |
| C. | 化学反应一定有能量变化,当△H为“-”时,表示该反应为吸热反应 | |
| D. | 已知C(s)+$\frac{1}{2}$O2(g)=CO(g)的反应热为-110.5kJ/mol,说明碳的燃烧热为110.5kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com