
����Ŀ���������ȣ�ClO2���Ǽ�������ˮ�Ҳ���ˮ������ѧ��Ӧ�Ļ���ɫ���壬�е�Ϊ11�棬ijС����ʵ�������Ʊ�ClO2����װ����ͼ��[��֪��SO2+2NaClO3+H2SO4=2ClO2+2NaHSO4]��
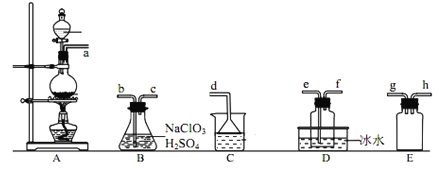
����˵����ȷ���ǣ� ��
A.װ��C��װ���DZ���ʳ��ˮ��a��������ΪSO2
B.װ��D�ű�ˮ��Ŀ����Һ�����������ֹ��Ⱦ����
C.����װ��ʱ�����ܿ�a�ɽ�h��g�����ܿ�c��e
D.����ѡ��װ��A����3mo/L������MnO2��Ӧ�Ʊ�����
���𰸡�C
��������
ClO2���Ʊ���װ��A����Cu��Ũ���ᷢ����Ӧ�Ʊ������������壬��װ��B�з������ɶ������ȵķ�Ӧ��Ϊ��ֹ������A��B֮������װ��E���������ȷе�ϵͣ�����D�б�ˮԡ�ռ��������������������δ��Ӧ��Ķ�������ֹ��Ⱦ�������ݴ˷������
A��װ��C������������SO2��β������ֹ��Ⱦ������Ӧѡ��NaOH��Һ����A����
B��װ��D������Ϊ�������ռ�ClO2����B����
C�����������a����װ��B�з�Ӧ��Ϊ��ֹ��������Ӧ��֮ǰ�а�ȫƿ����a��g��h��Ϊ��Ӧ��֣���������Bװ���е�b���������ȷе�ϵͣ�����D�б�ˮԡ�ռ���Ϊ�����ȴ�������ռ���������e�������������������δ��Ӧ��Ķ�������ֹ��Ⱦ����������˳��Ϊ��a��g��h��b��c��e��f��d����C��ȷ��
D��ʵ����������Ҫѡ��Ũ����Ͷ������̻�ϼ��ȣ�3mo/L�������ڼ���������MnO2��Ӧ����Cl2����D����
�ʴ�ΪC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ��2Ag+(aq)��Cu(s)=Cu2+(aq)��2Ag(s)��Ƶ�ԭ�����ͼ����ش��������⣺
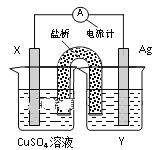
��1���缫X�IJ���������___���������ҺY���ʵĻ�ѧʽ��___��
��2�����缫Ϊ��ص�___���������ĵ缫��ӦΪ___��
��3�����·�еĵ����Ǵ�___�缫����___�缫��(��缫��������)��
��4������1.6gͭ�ܽ�ʱ����������___g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NAΪ�����ӵ�������ֵ����������������м����� ��
��BF3��CCl4������ԭ�Ӿ��ﵽ�����8�����ȶ��ṹ
��46g SiO2�к��й��ۼ�����ĿΪNA
��2g H218O��D2O�Ļ�����У����еĵ�����ΪNA
��K2SO4����ˮ�Ĺ����������Ӽ������ۼ��Ķ���
��78g Na2O2���������ӵ���ĿΪ4NA
��18g D2O����������10NA
��1mol NH5�к���5NA��N��H������֪NH5������ԭ�Ӷ��ﵽϡ��������ȶ��ṹ��
A.3B.4C.5D.6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һЩ�����л����ת����ϵ�����ڷ�Ӧ�١��ߵ�˵������ȷ���ǣ� ��

A. ֻ�з�Ӧ����������ӦB. ��Ӧ������ȥ��Ӧ
C. ֻ�з�Ӧ���ǼӳɾۺϷ�ӦD. ��Ӧ�ܢݢޢ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݷ��ӵĿռ�ṹ�ж�ԭ�ӹ��ߺ������⡢�ж����ʵ����ʺ�ͬ���칹����ѧϰ�л���ѧ������߱��Ļ��������������������⣺
��1�����з�Ӧ�IJ����У��е���ͬ���칹�壬�е�û��ͬ���칹�壬����һ��������ͬ���칹��ķ�Ӧ��______��
A �����ϩ(![]() )������ʵ�����Br2�����ӳɷ�Ӧ
)������ʵ�����Br2�����ӳɷ�Ӧ
B ���ǻ���������NaHCO3��Һ��Ӧ
C 2�ȶ�����NaOH�Ҵ���Һ���ȷ�����ȥHCl���ӵķ�Ӧ
D �ױ���һ�������·���������Ӧ����һ�����ױ��ķ�Ӧ
E �������������ڹ����·���һȡ����Ӧ
F ����������ϡ���������¼���ˮ��
��2��ij���ṹ��ʽ���£�![]() ���й���ṹ˵����ȷ������_______��
���й���ṹ˵����ȷ������_______��
A ����ԭ�ӿ�����ͬһƽ���� B ����ԭ�ӿ�����ͬһ��ֱ����
C ������ԭ�ӿ�����ͬһƽ���� D ����̼ԭ�ӿ�����ͬһƽ����
��3���л���A��һ�ֹ���ЧʳƷ����������ͼ��ʾ��A���ӵ����ģ�͡��ش��������⣺

����д��A�ķ���ʽ��_______��
����A�ܹ�������Ӧ��������(�����)��_________��
��������Ӧ �ڼӳɷ�Ӧ ��ȡ����Ӧ ����ȥ��Ӧ
����д��A���ռ���Һ��Ӧ�Ļ�ѧ����ʽ��___________��
��4��������һЩ�в�ҩ���������л��

���л�Ϊͬ���칹�����(�����)______��������ˮ��Ӧ����(�����)________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����ע�����м�������Na2SO3���壬����������Ũ����(�Բ��Ӵ�ֽ��Ϊ)���������й�˵����ȷ����(����)
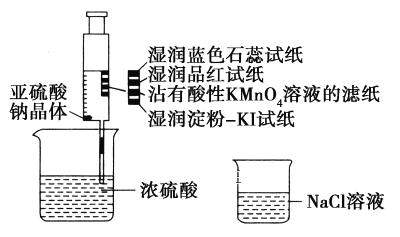
A. ��ɫʯ����ֽ�ȱ�����ɫ
B. Ʒ����ֽ��մ������KMnO4��Һ����ֽ����ɫ��֤��SO2����Ư����
C. ʪ����ۣ�KI��ֽδ����˵��SO2������������I2
D. NaCl��Һ�����ڳ�ȥʵ���ж����SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. 25 ��ʱ0.1molL��1NH4Cl��Һ��Kw����100��ʱ0.01molL��1NaCl��Һ��Kw
B. �����£�pH��Ϊ3�Ĵ����������������Һ�У���ˮ�������������Ũ��֮��Ϊ1��108
C. ������Һ��pH������ԵĹ�ϵ���Ƴ�pH��6.5����Һһ��������
D. �����£���pH��2��������pH��12�İ�ˮ�������ϣ���Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֡��������е���ĸ�ֱ����һ�ֻ�ѧԪ�ء�
a | b | ||||||||||||||||
[ | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o |
�����Ҫ����Ԫ�ط��Ż�ѧʽ�ش��������⣺
��1����������Ԫ���У�ԭ���������2�����ӵ�Ԫ��Ϊ_________��
��2������dԪ��ԭ�ӵĽṹʾ��ͼ_______________________________������̬�⻯������ˮ��_____________�ԡ���������������������
��3���Ƚ�Ԫ��g��Ԫ��h�γɵ�����������ˮ����ļ���ǿ��________��__________��
��4������jԪ����Ԫ�����ڱ��е�λ����______________________��
��5����������Ԫ���У�����������Ӧˮ���������ǿ����___________����д������Ļ�ѧʽ����ͬ�����������Ե���_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���������ԭ�ӵ��ӻ���ʽ�ͷ��ӵĿռ乹�;���ȷ����( ��
A. C2H2��sp2��ֱ����
B. SO42-��sp3��������
C. H3O+��sp3��V��
D. BF3��sp2��ƽ��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com