
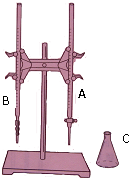
 ijͬѧ������ͼװ�ã���0.1000mol/L������������Һ�ⶨijδ֪Ũ�ȵ�������Һ�����ʵ���Ũ�ȣ�������ɷֽ�Ϊ���¼�����
ijͬѧ������ͼװ�ã���0.1000mol/L������������Һ�ⶨijδ֪Ũ�ȵ�������Һ�����ʵ���Ũ�ȣ�������ɷֽ�Ϊ���¼�����| ʵ����� | c��KOH��/mol?L-1 | B�����̶� | B���յ�̶� | V��HCl��/ml |
| 1 | 0.1000 | 0 | 24.95 | 25.00 |
| 2 | 0.1000 | 0 | 24.96 | 25.00 |
| 3 | 0.1000 | 0 | 24.50 | 25.00 |
| 4 | 0.1000 | 0 | 24.94 | 25.00 |
| c(KOH)��V(KOH) |
| V(HCl) |
| 24.95ml+24.96ml+24.94ml |
| 3 |
| c(KOH)��V(KOH) |
| V(HCl) |
| 0.1000mol/L��0.02495L |
| 0.02500L |


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ϳɰ���ҵ�У�����NH3����������Ӧ���ʣ����ԭ��ת���� |
| B������к͵ζ�ʱ����ƿ���ô���Һ��ϴ2�Σ��ټ������Һ |
| C����NO2��N2O4�����������ѹ��Ϊԭ����һ�룬��������ɫ���� |
| D���������������������������ֱ����Դ����������������Ӧ�õ��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��a=3 |
| B��a=2 |
| C��B��ת����Ϊ40% |
| D��B��ת����Ϊ60% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ɫ������Ӳ�Ⱥܴ� |
| B���������Ʒ���ʯ�������þƾ��Ƽ��Ⱥ����ƾ���ȼ�գ�������ɫ���棬����Na2O2 |
| C���������ڿ�����ȼ�գ����������� |
| D�������Ƶ��۵�ܸ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1-��ϩ |
| B���ױ� |
| C�����ױ� |
| D��2-��-3-�һ�-2-��ϩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
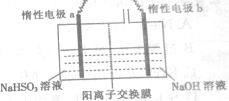 �����������ƣ�Na2S2O4���׳Ʊ��շۣ�����ǿ��ԭ�ԣ��㷺���ڷ�֯ƷƯ�����������ȣ�
�����������ƣ�Na2S2O4���׳Ʊ��շۣ�����ǿ��ԭ�ԣ��㷺���ڷ�֯ƷƯ�����������ȣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
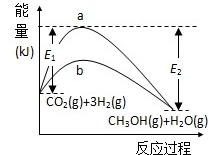 һ�������·�����Ӧ��
һ�������·�����Ӧ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com