
| A. | pH=1的溶液中,NO3-、Na+、I-、Fe2+ | |
| B. | pH=13的溶液中,Cl-、Mg2+、CH3COO-、K+ | |
| C. | 水电离出的c(H+)=1×10-12mol•L-1溶液中,HCO3-、SO42-、Na+、NH4+ | |
| D. | pH=14的无色透明溶液中,K+、Na+、NO3-、CO32- |
分析 A.pH=1的溶液呈强酸性溶液;
B.pH=13的溶液呈碱性;
C.水电离出的c(H+)=1×10-12mol•L-1溶液呈酸性或碱性;
D.pH=14的溶液呈强碱性,且溶液中不存在有色离子.
解答 解:A.pH=1的溶液呈强酸性溶液,酸性条件下NO3-和I-、Fe2+发生氧化还原反应而不能大量共存,故A错误;
B.pH=13的溶液呈碱性,Mg2+和氢氧根离子反应生成沉淀而不能大量共存,故B错误;
C.水电离出的c(H+)=1×10-12mol•L-1溶液呈酸性或碱性,强酸性或强碱性条件下,HCO3-都不能大量共存,强碱性条件下NH4+不能大量共存,故C错误;
D.pH=14的溶液呈强碱性,且溶液中不存在有色离子,这几种离子之间不反应且和氢氧根离子也不反应,且无色,所以能大量共存,故D正确;
故选D.
点评 本题考查离子的共存问题,明确离子之间的反应及复分解反应发生的条件、氧化还原反应即可解答,注意题干中限制性条件,易错选项是A.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
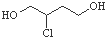 是一种中间产物,下列说法正确的是( )
是一种中间产物,下列说法正确的是( )| A. | 1,3-丁二烯与氢气加成产物只有一种 | |
| B. | 1,3-丁二烯转化为 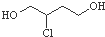 时,先与HCl发生1,2加成再水解得到 时,先与HCl发生1,2加成再水解得到 | |
| C. | 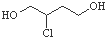 在NaOH醇溶液中或浓硫酸存在时加热都能发生消去反应 在NaOH醇溶液中或浓硫酸存在时加热都能发生消去反应 | |
| D. | 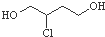 催化氧化得X,X能发生银镜反应,则X的结构只有两种 催化氧化得X,X能发生银镜反应,则X的结构只有两种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
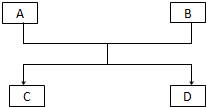 已知A、B、C、D的组成元素都属于短周期元素,其中A、D为单质,B、C为化合物,它们之间的关系转化如图所示,请按要求写出有关反应式,是离子反应的只写离子方程式.
已知A、B、C、D的组成元素都属于短周期元素,其中A、D为单质,B、C为化合物,它们之间的关系转化如图所示,请按要求写出有关反应式,是离子反应的只写离子方程式.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
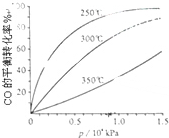 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 | |
| B. | 对2HI(g)?H2(g)+I2(g)平衡体系,增大平衡体系的压强可使颜色变深 | |
| C. | 反应CO+NO2?CO2+NO(正反应放热),升高温度可使平衡向逆反应方向移动 | |
| D. | 打开啤酒瓶盖后产生大量的气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充放电时,溶液中Pb2+浓度保持不变 | |
| B. | 放电时转移2mol电子,消耗2molPb | |
| C. | 放电时的负极反应式为:Pb-2e-═Pb2+ | |
| D. | 充电时的阳极反应式为:Pb2++4OH+2e-═PbO2+2HO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝与氢氧化钠反应 | |
| B. | 向氯化铝溶液中加入过量氨水 | |
| C. | 含氟牙膏中加入氯化铝并不断充分搅拌 | |
| D. | 向硫酸铜溶液中通入过量氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com