

 ��
������ I�����Һ������������Һ���ѵ��ʵԭΪI-�����Ȼ�̼������ˮ����ֲ㣬���Һ���ɵõ����Ȼ�̼��ʣ�����Һ�м���������I-�õ�I2�����������õ��ϴ���I2��
��1������������ԣ������������������������ƣ���������ԭ���ɵ⣻������ˮ����������������ˮ��
��2�����뻥�����ܵ�Һ����÷�Һ�ķ������룻
��3���������������������ܽ�������¶ȵ����߶���С�����������������ܺ�����������Һ��Ӧ���������ʣ�
II����1�������������£�I-��IO3-��Ӧ����I2��ˮ��I-ʧ���ӣ�IO3-�õ��ӣ��ݴ˷�����
��2���ٵ�һ����I-+3Br2+3H2O=6Br-+IO3-+6H+��
�ڵڶ�����IO3-+5I-+6H+=3I2+3H2O��
�ܵ��IJ���N2H4+2I2=4I-+N2��+4H+��
���ݷ�Ӧ��֮������ʵ�����ϵ�жϣ�
��� �⣺I�����Һ������������Һ���ѵ��ʵԭΪI-�����Ȼ�̼������ˮ����ֲ㣬���Һ���ɵõ����Ȼ�̼��ʣ�����Һ�м���������I-�õ�I2�����������õ��ϴ���I2��
��1������������ԣ������������������������ƣ���������ԭ���ɵ����ӣ����ӷ�Ӧ����ʽΪSO32-+I2+H2O=2I-+2H++SO42-��
������ˮ����������������ˮ��Ϊ��ʹ�����IԪ�ؽ���ˮ��ҺӦ���ԭΪ�����ӣ�
�ʴ�Ϊ��SO32-+I2+H2O=2I-+2H++SO42-��ʹCCl4�еĵ����ˮ�㣻
��2�����Ȼ�̼������ˮ������ֲ㣬���뻥�����ܵ�Һ����÷�Һ�ķ������룬���Է�������Ȼ�̼���÷�Һ�ķ������ʴ�Ϊ����Һ��
��3���������������������ܽ�������¶ȵ����߶���С���¶�Խ�ߣ��������ܽ��ԽС����ӦԽ����֣�����Ӧ���ڵ��������½��з�Ӧ�����������������ж�������ֱ���ſգ��Ҷ��ܺ�����������Һ��Ӧ���������ʣ�������NaOH��Һ���������͵�������
�ʴ�Ϊ��ʹ��������Һ���нϴ���ܽ�ȣ����ֹ���������ֹ���һ������������NaOH��Һ��
II����1�������������£�I-��IO3-��Ӧ����I2��ˮ��I-ʧ���ӣ�IO3-�õ��ӣ���Ӧ�ĵ���ת�Ƶķ������ĿΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2���ٵ�һ����I-+3Br2+3H2O=6Br-+IO3-+6H+��
�ڵڶ�����IO3-+5I-+6H+=3I2+3H2O��
�ܵ��IJ���N2H4+2I2=4I-+N2��+4H+��
��˴����Ϸ���ʽ�ͷ����ɵù�ϵʽ��I-��IO3-��3I2��6I-
1mol 6mol
��һ�Ρ���ѧ�Ŵ���Һ�I-������ԭ��Һ��I-������6����
���پ���һ�Ρ���ѧ�Ŵ�I-��IO3-��3I2��6I-
6mol 36mol
�����Ρ���ѧ�Ŵ���Һ�I-������ԭ��Һ��I-������36����
���Ծ���n�Ρ���ѧ�Ŵ���Һ�I-������ԭ��Һ�������6n����
�ʴ�Ϊ��6��6n��
���� ���⿼�������ʵķ����ᴿʵ�鷽����ƣ���ȷ���ʵ������ǽⱾ��ؼ����������ʵ��������ʡ�����������ᴿ������ѡȡ�ȷ������������֪����ļ��鷽������Ŀ�Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
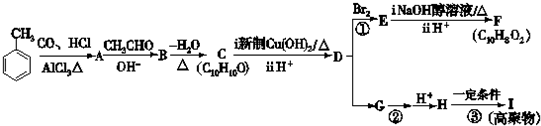
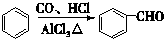
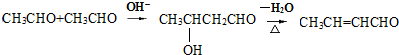
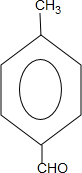 ��
�� +2Cu��OH��2$\stackrel{��}{��}$
+2Cu��OH��2$\stackrel{��}{��}$ +Cu2O��+2H2O��
+Cu2O��+2H2O�� $\stackrel{һ��������}{��}$
$\stackrel{һ��������}{��}$ +nH2O��
+nH2O�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ǽ���Ԫ��ԭ����ɵĻ����ﲻ���������ӻ����� | |
| B�� | ��A��Ԫ�صĽ�����һ���Ȣ�A��Ԫ�صĽ�����ǿ | |
| C�� | ͬһ����Ԫ����ɵĻ�����һ���ǹ��ۻ����� | |
| D�� | NH5�е�����ԭ�ӵ�����㶼������Ӧϡ������ԭ�ӵ��Ӳ�ṹ��1 mol NH5�к���4NA��N-H����NA��ʾ�����ӵ�������ֵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����ᣨH3PO2����һ�־�ϸ������Ʒ�����н�ǿ��ԭ�ԣ��ش��������⣺
�����ᣨH3PO2����һ�־�ϸ������Ʒ�����н�ǿ��ԭ�ԣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ���������Һ��һ��������Ϻ������ᾧ���� | |
| B�� | ����Һ�����������ӿ��Դ������棺H+��SO42-��I-��C6H5OH | |
| C�� | ����Һ������Ũ�ȴ�С��ϵΪ��SO42-��Fe3+��H+��OH- | |
| D�� | ����0.1 molNH4Fe��SO4��2��Һ�еμ�0.1 molBa��OH��2����Ӧ�����ӷ���ʽΪ��Fe3++2SO42-+2Ba2++3OH-=2BaSO4��+Fe��OH��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10��20 mL 3mol/L��X��Һ | B�� | 20��30 mL 2molL��X��Һ | ||
| C�� | 20��10 mL 4mol/L��X��Һ | D�� | 10��10 mL 2mol/L��X��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com