
【题目】实验室用下列方法测定某水样中O2的含量。
(1)实验原理。
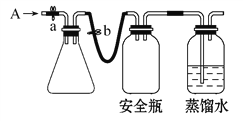
①用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为____________________________。
②在酸性条件下,再用I-将生成的MnO(OH)2还原为Mn2+,反应的离子方程式为____________________。然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为I2+2Na2S2O32NaI+Na2S4O6。
(2)实验步骤。
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是_________;
②用注射器抽取某水样20.00 mL从A处注入锥形瓶;
③再分别从A处注入含mmol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及一定浓度的硫酸(含H2SO4nmol);
⑥重复④的操作;
⑦取下锥形瓶,向其中加入2~3滴__________作指示剂;
⑧用0.005 mol·L-1Na2S2O3溶液滴定至终点。滴定终点的现象是_____________。
(3)数据分析。
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________mg·L-1。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将__________(填“偏大”“偏小”或“不变”)。
③实验要求加入适量的H2SO4使溶液接近中性,其原因是__________________。
【答案】 2Mn2++O2+4OH-2MnO(OH)2 MnO(OH)2+2I-+4H+Mn2++I2+3H2O 排出装置内的空气,避免空气中O2的干扰 淀粉溶液 滴入最后一滴标准液,溶液恰好由蓝色变为无色,且半分钟内不恢复原色 7.8 偏大 若碱过量,则MnO(OH)2不能全部转变为Mn2+,而酸过量时,滴定过程中Na2S2O3可与酸反应
【解析】试题分析:(1)① O2与Mn2+反应生成MnO(OH)2,根据得失电子守恒、电荷守恒配平方程式;I-与MnO(OH)2反应生成Mn2+和碘单质,根据得失电子守恒、电荷守恒配平方程式;(2)① 装置内的空气中含有氧气干扰实验;⑦根据反应中有碘单质参与,利用淀粉遇碘单质变蓝的性质,选择淀粉作指示剂;⑧滴定终点时碘单质完全被消耗,溶液由蓝色变为无色;(3)①根据关系式2Na2S2O3![]() I2
I2 ![]() MnO(OH)2
MnO(OH)2![]()
![]() O2计算水样中O2的含量;②若未用Na2S2O3标准溶液润洗滴定管,Na2S2O3的浓度偏小,消耗Na2S2O3的体积偏大;③若碱过量,则MnO(OH)2不能全部转变为Mn2+,而酸过量时,滴定过程中Na2S2O3可与酸反应。
O2计算水样中O2的含量;②若未用Na2S2O3标准溶液润洗滴定管,Na2S2O3的浓度偏小,消耗Na2S2O3的体积偏大;③若碱过量,则MnO(OH)2不能全部转变为Mn2+,而酸过量时,滴定过程中Na2S2O3可与酸反应。
解析:(1)① O2与Mn2+反应生成MnO(OH)2,根据得失电子守恒、电荷守恒配平方程式得2Mn2++O2+4OH-2MnO(OH)2;I-与MnO(OH)2反应生成Mn2+和碘单质,根据得失电子守恒、电荷守恒配平方程式得MnO(OH)2+2I-+4H+Mn2++I2+3H2O;(2)① 装置内的空气中含有氧气,从A处向装置内鼓入过量N2的目的是排出装置内的空气,避免空气中O2的干扰;⑦根据反应中有碘单质参与,利用淀粉遇碘单质变蓝的性质,选择淀粉作指示剂;⑧滴定终点时碘单质完全被消耗,滴定终点的现象是滴入最后一滴标准液,溶液恰好由蓝色变为无色,且半分钟内不恢复原色;
(3)① 设1000mL水样中含有氧气n mol
根据关系式2Na2S2O3![]() I2
I2 ![]() MnO(OH)2
MnO(OH)2![]()
![]() O2 ;
O2 ;
n (I2)=![]() =
=![]() mol, O2的质量是
mol, O2的质量是![]() 7.8mg;所以氧气的含量是7.8mg·L-1;②若未用Na2S2O3标准溶液润洗滴定管,Na2S2O3的浓度偏小,消耗Na2S2O3的体积偏大,所以测得水样中O2的含量将偏大;③若碱过量,则MnO(OH)2不能全部转变为Mn2+,而酸过量时,滴定过程中Na2S2O3可与酸反应。
7.8mg;所以氧气的含量是7.8mg·L-1;②若未用Na2S2O3标准溶液润洗滴定管,Na2S2O3的浓度偏小,消耗Na2S2O3的体积偏大,所以测得水样中O2的含量将偏大;③若碱过量,则MnO(OH)2不能全部转变为Mn2+,而酸过量时,滴定过程中Na2S2O3可与酸反应。


科目:高中化学 来源: 题型:
【题目】制备硅单质时,主要化学反应如下:
(1)SiO2+2C ![]() Si+2CO↑
Si+2CO↑
(2)Si+2Cl2 ![]() SiCl4
SiCl4
(3)SiCl4+2H2 ![]() Si+4HCl
Si+4HCl
下列对上述三个反应的叙述中,不正确的是( )
A.(1)(3)为置换反应
B.(1)(2)(3)均为氧化还原反应
C.(2)为化合反应
D.三个反应的反应物中硅元素均被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Na和Na+的叙述中,错误的是( )
A. 它们相差一个电子层 B. 钠原子、钠离子均为同一元素
C. 它们的化学性质相似 D. 灼烧时,它们的焰色反应都呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制取氨气的气体发生装置,请
结合所学知识,回答下列问题: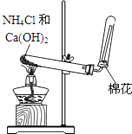
(1)图中用于加热的仪器名称是 , 收集氨气的方法是法.验证氨气是否已经收集满的方法是(任写一种).
(2)写出实验室制取氨气的化学方程式:
(3)若有5.35g氯化铵参加反应,则产生的氨气在标准状况下的体积为L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 煤和石油都是可再生资源 B. 分离煤焦油可以获取苯
C. 石油的裂化仅能得到烷烃 D. 煤的气化和石油的分馏都属于物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应式:⑴2Fe3+ + 2I- = 2Fe2+ + I2 ⑵Br2 + 2Fe2+ = 2Br- + 2Fe3+可判断离子的还原性由强到弱的顺序是( )
A. Br-、Fe2+、I- B. Br-、I-、Fe2+ C. I-、Fe2+、Br- D. Fe2+、I-、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列4组物质均有一种物质的类别与其它3种不同
A.CaO、Na2O、CO2、CuO B. H2、C.P、Cu
C.O2、Fe、Cu、Zn D. HCl、H2O、H2SO4、HNO3
以上四组中与其它3种类别不同的物质依次是(填化学式)
A ; B ; C ; D 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在其他条件不变的情况下,升高温度,下列数值不一定增大的是( )
①水解平衡常数 ②化学平衡常数 ③电离平衡常数 ④物质的溶解度
A.②③B.①④C.③④D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组利用废旧铝铜合金(含有少量杂质铁)制备Al(OH)3,流程如下:

回答下列问题:
(1)铝铜合金很坚硬,轻而抗张强度大,可代替昂贵的铜线为电线。但该合金暴露在空气中易被腐蚀,原因是___________________________。
(2)废旧铝铜用过量的稀硫酸浸取时,发生反应的化学方程式为________________。
(3)能溶解滤渣A而不产生空气污染的方法是___________________。
(4)在温度为358~368K时,加入Al2O3调节pH=1.6~1.8,析出黄铁矾[Na2Fe6(SO4)4(OH)12]。写出析出黄铁矾的离子方程式
(5)加NH3·H2O后将沉淀经过滤、_________、_________称量,得Al(OH)3质量为废旧铝铜合金质量的2.6 倍,则废旧铝铜合金含中Al的质量分数≤________%。
(6)Al(OH)3是塑料和有机聚合物的一种理想的阻燃剂填充料。塑料或聚合物与外部热源接触而燃烧时,可分为以下几个阶段:①加热,②分解,③起火,④燃烧,⑤蔓延。Al(OH)3阻燃起作用的阶段是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com