
室温下,下列各组离子在指定溶液中能大量共存的是( )
A. c(H+)=0.1mol/L的溶液:Na+、NH4+、SO42﹣、S2O32﹣
B. 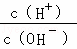 =1×10﹣12的溶液:K+、AlO2﹣、CO32﹣、Na+
=1×10﹣12的溶液:K+、AlO2﹣、CO32﹣、Na+
C. 在由水电离出的c(H+)=1×10﹣12mol/L的溶液:Fe3+、ClO﹣、Na+、SO42﹣
D. c(Fe2+)=0.1mol/L的溶液:H+、Al3+、NO3﹣、SCN﹣
考点: 离子共存问题.
分析: A、在酸性条件下S2O32﹣发生自身的氧化还原反;
B、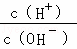 =1×10﹣12<1,溶液呈碱性;
=1×10﹣12<1,溶液呈碱性;
C、由水电离出的c(H+)=1×10﹣12mol/L的溶液,说明水的电离平衡受抑制,溶液可能是酸性溶液,也可能是碱性溶液;
D、氢离子、硝酸根离子构成强氧化性体系,氧化亚铁离子.
解答: 解:A、在酸性条件下S2O32﹣发生自身的氧化还原反,生成二氧化硫和单质硫,故A错误;
B、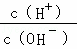 =1×10﹣12<1,溶液呈碱性,该组离子之间不反应,可大量共存,故B正确;
=1×10﹣12<1,溶液呈碱性,该组离子之间不反应,可大量共存,故B正确;
C、由水电离出的c(H+)=1×10﹣12mol/L的溶液,说明水的电离平衡受抑制,溶液可能是酸性溶液,也可能是碱性溶液,酸性溶液中ClO﹣不能稳定存在,碱性溶液中,铁离子与氢氧根离子结合生成难溶的氢氧化铁,故C错误;
D、氢离子、硝酸根离子构成强氧化性体系,氧化亚铁离子,所以离子间不能大量共存,故D错误;
故选B.
点评: 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子的反应为解答的关键,侧重分析能力与氧化还原反应、复分解反应的考查,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:
下列说法不科学的是( )
A. 自然界“水滴石穿”的主要原因用方程式表示为:CaCO3+H2O+CO2═Ca(HCO3)2
B. “雨后彩虹”是与胶体、光学等知识有关的自然现象
C. 人类目前直接利用的能量大部分是由化学反应产生的
D. “生物固氮”是指植物通过叶片直接吸收空气中的氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | 过量的NaHSO4与Ba(OH)2溶液反应 Ba2++OH﹣+H++SO42﹣═BaSO4↓+2H2O |
|
| B. | NH4HCO3溶液与过量的NaOH溶液反应 NH4++OH﹣═NH3↑+H2O |
|
| C. | 苯酚钠溶液中通入少量CO2 |
|
| D. | FeBr2溶液中通入过量Cl2 2Fe2++2Br﹣+2Cl2═2Fe3++Br2+4Cl﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁是4种短周期元素,它们的原子序数依次增大,其中甲和丙、乙和丁分别是同主族元素,又知乙、丁两元素的原子核中质子数之和是甲、丙两元素的原子核中质子数之和的2倍,甲元素的一种核素核内无中子.
(1)丙、丁组成的常见化合物,其水溶液呈碱性,原因是
(用离子方程式表示);
写出两种均含甲、乙、丙、丁四种元素的化合物相互间发生反应,且生成气体的离子方程式 .
(2)丁的单质能跟丙的最高价氧化物的水化物的浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式 .
(3)甲、乙、丁可形成A、B两种微粒,它们均为﹣1价双原子阴离子,且A有18个电子,B有10个电子,则A与B反应的离子方程式为 .
(4)4.0g丁单质在足量的乙单质中完全燃烧放出37.0kJ热量,写出其热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各选项中的两个反应,可用同一个离子方程式表示的是( )
选项 Ⅰ Ⅱ
A Ba(OH)2溶液与过量NaHCO3溶液混合 NaOH溶液与过量NaHCO3溶液混合
B 少量SO2通入Ba(OH)2溶液中 过量SO2通入Ba(OH)2溶液中
C BaCl2溶液与Na2SO3溶液混合 Ba(OH)2溶液与H2SO3溶液混合
D 少量氨水滴入AlCl3溶液中 少量AlCl3溶液滴入氨水中
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4═2CuI↓+13I2+12K2SO4+12H2O,下列说法正确的是( )
A. Cu(IO3)2作氧化剂,Cu(IO3)2中的铜和碘元素被还原
B. CuI既是氧化产物又是还原产物
C. 每生成1 mol CuI,有12 mol KI发生氧化反应
D. 每转移1.1 mol电子,有0.2 mol 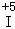 被氧化
被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一.下列说法正确的是( )
A. 给试管中的铜与浓硫酸加热,发现试管底部有白色固体并夹杂有少量黑色物质,此白色固体为硫酸铜,黑色固体为氧化铜
B. 浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸
C. 相同质量的铜分别与足量的等体积的浓硝酸和稀硝酸反应,生成溶液分别为绿色和蓝色,是由于反应时产生的铜离子浓度前者大于在后者
D. 将铜片放入浓硫酸中,无明显实验现象,说明铜在冷的浓硫酸中发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要使用玻璃棒,其中玻璃棒作用相同的是( )
①过滤;②蒸发;③溶解;④向容量瓶中转移液体.
A. ①和④ B. ①和③ C. ③和④ D. ①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
想一想:Ba(OH)2(固体)、CuSO4(固体)、纯醋酸(液态)这些物质为什么归为一类,下列哪些物质还可以和它们归为一类( )
|
| A. | 75%的酒精溶液 | B. | 硝酸钠晶体 |
|
| C. | Fe(OH)3胶体 | D. | 豆浆 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com