
(16分)中学化学常见的物质A、B、C、D之间存在如下转化关系:A + B →C+D + H2O(没
有配平)请按要求填空:
(1)若A为短周期元素组成的黑色固体单质,与B的浓溶液共热时,产生C、D两种气体。C、D两种气体均能使澄清石灰水变浑浊,则该反应的化学方程式是:______________________,鉴别这两种气体不能选用的试剂是___________。
a.BaCl2溶液 b.KMnO4溶液 c.品红溶液 d.酸化的Ba(NO3)2溶液
向500mL 2mol?L-1的NaOH溶液中通入0.8mol无色无味的C气体,恰好反应完全,此时反应混合液中物质的量最大的微粒是 ;此时溶液中的阴离子按照浓度由大到小排列的顺序是______。
(2)若A与适量B的溶液在常温下恰好完全反应,生成的无色气体C遇空气迅速变成红棕色,将生成的红棕色气体通入一个烧瓶里,塞紧瓶塞后,将烧瓶浸入冰水中,烧瓶中气体的颜色变浅,请用化学方程式和必要的文字解释颜色变化的原因_______________________________。
(3)若A在水中的溶解度随温度的升高而降低;B为短周期非金属单质,C是漂白粉的有效成分之一,C发生水解反应的离子方程式是______________________________。
(1)C + 2H2SO4(浓)△CO2↑ + 2SO2↑ + 2H2O (3分) a(2分) n(H2O)(2分)
c(HCO3-)>c(CO3 2- )>c(OH-)(2分) (2)2NO2(g) N2O4(g) △H<0(2分)
N2O4(g) △H<0(2分)
降温,平衡向正反应方向移动,红棕色NO2浓度减小,混合气体的颜色变浅 (2分)
(3)ClO-+H2O HClO+OH-(3分)
HClO+OH-(3分)
解析试题分析:(1)C、D两种气体均能使澄清石灰水变浑浊,为SO2、CO2,A为短周期组成的黑色固体物质,与B的浓溶液共热时,产生SO2、CO2两种气体,同时生成水,A为C单质,B为浓硫酸,符合转化关系;碳与浓硫酸在加热的条件下生成SO2、CO2、水,反应方程式为:C + 2H2SO4(浓)△CO2↑ + 2SO2↑ + 2H2O。a、SO2、CO2都不能与氯化钡溶液反应,无法区别,故a错误;b、SO2能被酸性高锰酸钾溶液氧化,使酸性高锰酸钾褪色,CO2不能反应,可以鉴别,故b正确;c、SO2能品红溶液褪色,CO2不能使品红溶液褪色,可以鉴别,故c正确;d、酸化的硝酸钡溶液通入SO2,可以氧化亚硫酸钡为硫酸钡,产生白色沉淀,通入CO2不反应,可以鉴别,故d正确;故A不能鉴别;CO2的物质的量0.8mol,500mL2mol/L NaOH的水溶液中n(NaOH)=0.5L×2mol/L=1mol,n(CO2):n(NaOH)=0.8mol:1mol=2:3=1:1.25,介于1:1与1:2之间,故反应生成碳酸钠与碳酸氢钠,令碳酸钠与碳酸氢钠的物质的量分别为amol、bmol,由钠离子守恒有2a+b=1,由碳元素守恒有a+b=0.8,联立方程,解得a=0.2,b=0.6,反应离子方程式为:4CO2+5OH-=CO32-+3HCO3-+2H2O;碳酸根、碳酸氢根水解,溶液呈碱性c(OH-)>c(H+),碳酸根的水解程度比碳酸氢根的大,但水解程度很小,故c(HCO3-)>c(CO32-),c(CO32-)原大于c(OH-),溶液中钠离子难度最大,但此反应混合液中物质的量最大的微粒是水,溶液中的阴离子按照浓度由大到小排列的顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)。
(2)若A与适量B的溶液在常温下恰好完全反应,生成的无色气体C遇空气迅速变成红棕色,说明C是NO,红棕色气体是NO2。二氧化氮与四氧化二氮存在平衡关系2NO2(g) N2O4(g) △H<0,正方应是放热反应,降温,平衡向正反应方向移动,红棕色NO2浓度减小,混合气体的颜色变浅。
N2O4(g) △H<0,正方应是放热反应,降温,平衡向正反应方向移动,红棕色NO2浓度减小,混合气体的颜色变浅。
(3)若A在水中的溶解度随温度升高而降低,考虑A为Ca(OH)2,B为短周期非金属单质,D是漂白粉的成分之一,B为Cl2,符合转化关系与题意,D能发生水解故D为Ca(ClO)2,Ca(ClO)2发生水解的离子方程式为:ClO-+H2O HClO+OH-。
HClO+OH-。
考点:考查无机框图题的推断


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:单选题
下列根据操作和现象或目的所得出的结论正确的是
| 选项 | 操作 | 现象或目的 | 结论 |
| A | 工业上,将BaSO4浸泡在饱和Na2CO3溶液中 | 将BaSO4转化为BaCO3 | Ksp(BaSO4)>Ksp(BaCO3) |
| B | 向NaAlO2溶液中滴入NaHCO3 | 有白色沉淀 | AlO2-结合H+能力比CO32-强 |
| C | 向PbO2中滴入浓盐酸 | 有黄绿色气体 | PbO2具有还原性 |
| D | 向鸡蛋白溶液中滴入HgCl2溶液 | 有白色沉淀 | 蛋白质发生盐析 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.Na2O2可作为潜艇工作人员的供氧剂 |
| B.常温下铝箔放在浓HNO3中,生成H2 |
| C.水蒸气通过炽热的铁,生成Fe(OH)3和H2 |
| D.用新制Cu(OH)2检查尿糖,Cu(OH)2是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验过程中会先产生白色沉淀后沉淀又溶解的是( )
| A.向AlCl3溶液中滴加氨水至过量 |
| B.向Ba(NO3)2溶液通入SO2至过量 |
| C.向Ba(0H)2溶液通入CO2至过量 |
| D.向新制Fe(OH)3胶体中滴加稀硫酸至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关物质的性质和该性质的应用均正确的是
| A.H2O2是一种绿色氧化剂,可与酸性高锰酸钾作用产生 |
| B.SiO2晶体硅具有半导体性质,可用于生产光导纤维 |
| C.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸 |
| D.铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氢气是一种清洁能源,氢气的制取与储存是氢气能源利用领域的研究热点。
已知:CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH =+206.2 kJ·mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH =+247.4 kJ·mol-1
2H2S(g)=2H2(g)+S2(g)ΔH =+169.8 kJ·mol-1
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与 H2O(g)反应生成CO2(g)和 H2(g)的热化学方程式为_________________________
(2)H2S 热分解制氢时,常向反应器中通入一定比例空气,使部分 H2S 燃烧,其目的是________;燃烧生成的 SO2与 H2S 进一步反应,生成物在常温下均为非气体,写出该反应的化学方程式:___________________________
(3)H2O 的热分解也可得到 H2,高温下水分解体系中主要气体的体积分数与温度的关系如图甲所示。图中 A、B 表示的物质依次是______________________________________。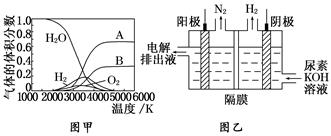
(4)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图乙(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为_____________________
(5)Mg2Cu 是一种储氢合金。 350 ℃时,Mg2Cu 与 H2反应,生成 MgCu2和仅含一种金属元素的氢化物(其中氢的质量分数为 0.077)。Mg2Cu 与 H2反应的化学方程式为_____________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知X、Y、Z、M、Q、G、R、T,前四周期的8种元素(未按照原子序数排列),Z元素的某种氢化物可用作火箭的燃料;Q元素的单质为绿色植物光合作用的一种产物;根据化学对角线法则,G元素对角线的另一种元素T的单质可溶于R元素最高价氧化物所对应水溶液中并且目前易拉罐包含G元素最多;Y元素的价电子排布式为(n+1)Sn (n+1)P(n+3); X元素某种的盐溶液可以与M元素的单质发生反应,并能生成X元素的单质,且两者核电荷数相差3,且M元素的单质是地壳含量第二高的金属元素;R元素为第三周期的某种元素。
(1)写出X元素的价电子排布式 ,Z元素对应的最简单氢化物的空间构型 。
(2)写出元素T的单质可溶于R元素最高价氧化物所对应水溶液对应的离子方程式:
。
(3)Q元素所对应的氢化物的沸点比同主族元素所对应氢化物沸点高的原因是:
。
(4)生活中,应将含Y、Q元素的某种粉末状物质密封、避光、干燥保存,且该粉末状物质经常在洗衣服时用到,请用化学方程式说明,该物质敞放在空气失效的原因:
。
(5)Z元素的某种氢化物,可用作火箭燃料,且该化合物中Z原子与氢原子的个数比为1:2,工业上用尿素和漂白液的主要有效成分,在R元素最高价氧化物所对应水溶液中并用高锰酸钾作为催化剂反应生成这种名为水合氨的化合物,生成的其它产物中某种离子,可以与CaCl2溶液反应生成某种白色沉淀,大理石中主要含这种成分。通过以上资料,写出该化学方程式:
。
(6)若取M元素的某种氧化物于试管中,加入稀盐酸调pH约为7,加入淀粉-KI溶液和Q元素的某种化合物,且该化合物的空间构型为异面折线形,反应完后溶液呈蓝色并有红褐色沉淀生成。当消耗2mol I-时,共转移3mol电子,该反应的离子方程式:
。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某同学设计如图装置,研究非金属元素性质变化规律.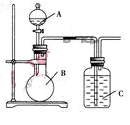
(1)已知硅酸(H2SiO3)是一种难溶于水的弱酸,呈白色。在化学反应中,一般地,强酸能制弱酸,如NaHCO3+HCl=NaCl+CO2↑+H2O,得出:HCl酸性强于H2CO3的酸性。现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:酸性:HNO3>H2CO3>H2SiO3。
A中装试剂________,B中装试剂____________,C中装试剂____________。C中实验现象为____________;写出C中发生反应的离子方程式_____________________________。
(2)已知高锰酸钾在常温下与浓盐酸反应产生氯气,利用如图装置证明氯气氧化性强于碘单质的氧化性。则A中装浓盐酸,B中装入高锰酸钾粉末,C中装试剂________,C中现象________,写出离子方程式__________________。该实验装置有明显不足,请指出改进方法:_______________________________________。
(3)如果C中装饱和的氢硫酸溶液,A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察到现象是C中产生淡黄色沉淀,写出化学方程式______________________________;证明氯的非金属性比硫的非金属性________(填“强”或“弱”或“无法判断”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com