
【题目】取氯化钠和碳酸钠的混合固体13.9g,加入50g水使其完全溶解,滴入90.5g稀盐酸恰好完全反应,反应后所得溶液质量为150g,请计算:
(1)完全反应后,生成CO2的质量为 g。
(2)混合物中碳酸钠的质量分数。
(3)反应后所得溶液中溶质的质量分数。(Na2CO3+2HCl=2NaCl+CO2↑+H2O).
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F原子序数依次增大.A的阳离子就是一个质子:B原子的最外层电子数是所在周期数的2倍;C、D在周期表中处于相邻位置,它们的单质在通常状况下均为无色气体:E与A同一主族:F原子的K、L层电子数之和比K、M层电子数之和多l。A、D、E三种元素可形成化合物甲,B、D、E三种元素可形成化合物乙。请回答:
(1)C2的结构式为_______________。
(2)由上述元素组成的既含极性健又含非极性键的无机化合物分子的电子式为__________。
(3)A的单质与D的单质在强酸性条件下构成燃料电池,其正极反应式为__________。
(4)常温下,甲与乙的水溶液pH均为9,这两种溶液中由水电离出的OH-的物质的量浓度c(OH -)甲:c(OH-)乙= ________。
(5)将2.4gB的单质在足量D的单质中燃烧,所得气体通入1L 0.3mol/L的甲溶液中,完全吸收后,溶液中的溶质为______。溶液中所含离子的物质的量 浓度由大到小的顺序为______。
(6)由A、B、C、D四种元素组成的无机酸的酸式盐,与足量的NaOH溶液在加热条件下反应的离子方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应进行到一定程度会达到化学平衡状态,如K2Cr2O7溶液中存在平衡:Cr2![]() (橙色)+H2O
(橙色)+H2O![]() 2Cr
2Cr![]() (黄色)+2H+。平衡时各种物质含量保持不变,达到一种相对的静止(如平衡时,每消耗1molH2O同时也会生成1molH2O)。外界条件改变时,平衡状态会被破坏而发生移动(如消耗的水多于生成的水,则平衡向正向移动),平衡移动符合勒夏特列原理,即如果改变可逆反应的条件(如浓度、压强、温度等),化学平衡就被破坏,并向减弱这种改变的方向移动。现在用K2Cr2O7溶液进行下列实验:
(黄色)+2H+。平衡时各种物质含量保持不变,达到一种相对的静止(如平衡时,每消耗1molH2O同时也会生成1molH2O)。外界条件改变时,平衡状态会被破坏而发生移动(如消耗的水多于生成的水,则平衡向正向移动),平衡移动符合勒夏特列原理,即如果改变可逆反应的条件(如浓度、压强、温度等),化学平衡就被破坏,并向减弱这种改变的方向移动。现在用K2Cr2O7溶液进行下列实验:

已知:C2H5OH遇到氧化剂容易被氧化。
结合实验,下列说法不正确的是 ( )
A. ①中溶液橙色加深,③中溶液变黄 B. ②中Cr2![]() 被C2H5OH还原
被C2H5OH还原
C. 对比②和④可知K2Cr2O7酸性溶液氧化性弱 D. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气和二氧化氮气体在室温下可以化合生成一种新的气态化合物A,为了测定A的组成进行以下实验,取Cl2、NO2混合气总体积5L,测定反应后所得气体体积随Cl2在原混合气体中所占体积分数x的变化而变化的规律.实验测知当Cl2所占体积分数为0.2或0.6时,反应后的总体积均为4L.
(1)通过分析和计算求得化合物A的化学式为_______________________________,发生反应的化学方程式_______________________________________________________.
(2)试讨论当x的取值范围不同时,反应后总体积V随x变化的函数关系_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关工业生产的叙述中错误的是
A. 电解氯化钠溶液制金属钠
B. 石灰石是炼铁和制玻璃的原料之一
C. 氯气通入石灰乳中制漂白粉
D. 硫酸工业的主要设备有沸腾炉、接触室、吸收塔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A处通入氯气,打开B阀时,C处红色布条不褪色;关闭B阀时,C处红色布条褪色;由此作出的判断正确的是( )
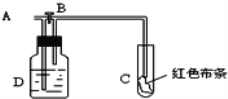
A. D中可能是浓硫酸
B. 通入的氯气含有水蒸气
C. D中可能是水
D. D中可能是NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO-
B.双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O
C.用铜作电极电解CuSO4溶液:2Cu2++2H2O![]() 2Cu+O2↑+4H+
2Cu+O2↑+4H+
D.Na2S2O3溶液中加入稀硫酸:2S2O32—+4H+=SO32—+3S↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用相关原理,回答下列各小题:
I.已知:NaHSO4在水中的电离方程式为NaHSO4=Na++H++SO42- .
(1)常温下,pH=5的NaHSO4溶液中水的电离程度______________(填“>”、”=”或“<”)pH=9的氨水中水的电离程度。
(2)等体积等物质的量浓度的NaHSO4与氨水混合后,溶液呈酸性的原因为:______________(用离子方程式表示);若一定量的NaHSO4溶液与氨水混合后,溶液pH=7,则c(Na+)+c(NH![]() )______________c(SO42-)(填“>”、“=”或“<”);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH______________7(填“>”、”=”或“<”)。
)______________c(SO42-)(填“>”、“=”或“<”);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO42-完全沉淀,则反应后溶液的pH______________7(填“>”、”=”或“<”)。
(3)将分别含有MnO![]() 、Fe3+、Fe2+、I- 的四种溶液混合,调节溶液的pH,使pH=1,充分反应后:若I- 离子有剩余,上述四种离子在溶液中还存在的有______________,一定不存在的是______________。
、Fe3+、Fe2+、I- 的四种溶液混合,调节溶液的pH,使pH=1,充分反应后:若I- 离子有剩余,上述四种离子在溶液中还存在的有______________,一定不存在的是______________。
II.在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl,利用Ag+与CrO42生成砖红色沉淀,指示到达滴定终点。当溶液中Cl恰好沉淀完全(浓度等于1.0×105 mol·L1)时,溶液中c(Ag+)为________________mol·L1,此时溶液中c(CrO42)等于______________mol·L1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×1012和2.0×1010)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活息息相关。下列各“剂”在应用过程中表现还原性的是( )
A. 臭氧柜里臭氧作餐具的“消毒剂” B. 热纯碱溶液常作厨房的“洗涤剂”
C. 活性铁粉在食品袋中作“去氧剂” D. 小苏打常作制糕点的“起泡剂”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com