
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子的还原性强弱:Fe2+>Br->Cl- | |
| B. | 当氯气少量时,发生的离子反应:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 当a=b时,反应后溶液的离子浓度:c(Fe3+):c(Br-):c(Cl-)=1:2:2 | |
| D. | 当氯气过量时,发生离子反应:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
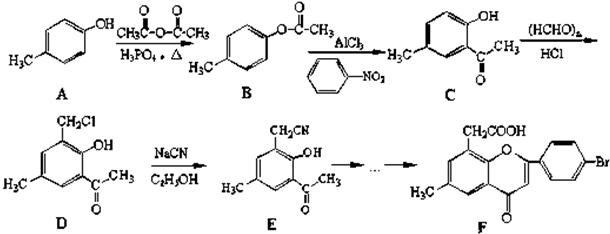
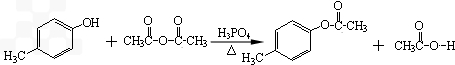 .
.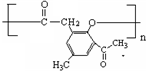 .
.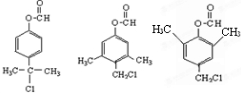 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
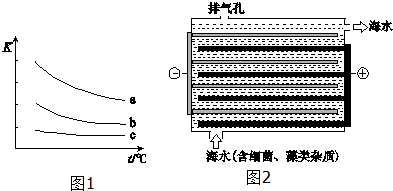
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 往Fe(OH)3胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解 | |
| C. | 纳米材料粒子直径一般从几纳米到几十纳米,因此纳米材料属于胶体 | |
| D. | 水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘粒子带电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(4)(5) | B. | (2)(5) | C. | (1)(3) | D. | (2)(3)(5) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,17gH2O2中含极性键的数目为NA | |
| B. | 1L 1mo/L的Fe2(SO4)3溶液中含有的硫酸根离子数为3NA | |
| C. | 标准状况下,11.2LN2和H2的混合气体中所含原子数为NA | |
| D. | 5.6gFe溶于1L 0.3moL/L硝酸中,转移的电子数为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com