
| A. | 10gH2和10gCO | B. | 11.2LCO(标准状况)和22gCO2 | ||
| C. | 18gH2O和44gCO2 | D. | 22.4LH2和0.1molN2 |
分析 各组物质中所含分子数相等,则各物质的物质的量相等,根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算各物质小于的物质的量,注意D选项中氢气不一定处于标况下,不能确定其物质的量.
解答 解:A.氢气与CO的摩尔质量不相等,根据n=$\frac{m}{M}$可知10gH2和10gCO的物质的量不相等,而二者含有分子数目不相等,故A错误;
B.标况下11.2L CO物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,22gCO2的物质的量为$\frac{22g}{44g/mol}$=0.5mol,二者含有分子数目相等,故B正确;
C.18gH2O的物质的量为$\frac{18g}{18g/mol}$=1mol,44gCO2的物质的量为$\frac{44g}{44g/mol}$=1mol,二者含有分子数目相等.故C正确;
D.氢气不一定处于标况下,22.4LH2的物质的量不一定为0.1mol,与0.1molN2含有分子数目不一定相等,故D错误.
故选:BC.
点评 本题考查物质的量有关计算,注意气体摩尔体积的使用条件与对象,根据PV=nRT理解温度、压强对气体摩尔体积的影响.


科目:高中化学 来源: 题型:解答题
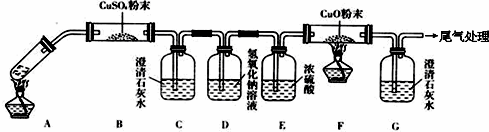
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
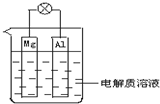 如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、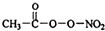 (PAN)等二次污染物.
(PAN)等二次污染物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④⑤ | C. | ①③ | D. | ②④⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
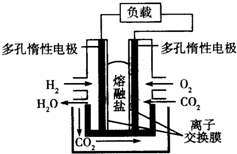
| A. | CO2在电池反应过程中不参与反应 | |
| B. | 电池总反应为2H2O═O2↑+2H2↑ | |
| C. | 该离子交换膜为阳离子交换膜 | |
| D. | 电池正极反应式为O2+2CO2+4e-═2CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com