
【题目】辉铜矿(主要成分是Cu2S)含铜量高,是最重要的炼铜矿石。
I.已知: ①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) △H=-768.2kJ.mol-1
②Cu2S(s)+O2(g)=2Cu(s)+SO2(g) △H=-217.4kJ.mol-1
(1)Cu2S与Cu2O反应生成Cu和SO2的热化学方程式为_____________。
Ⅱ.Cu2O可催化二甲醚合成乙醇。
反应①:CH3OCH3(g)+CO(g)![]() CH3COOCH3(g) △H1
CH3COOCH3(g) △H1
反应②:CH3COOCH3(g)+2H2(g)![]() CH3OH(g)+C2H5OH(g) △H2
CH3OH(g)+C2H5OH(g) △H2
(2)压强为pkPa时,温度对二甲醚和乙酸甲酯平衡转化率的影响如图1所示,则△H1____(填“>”或“<”,下同)0、△H2_____0。温度对平衡体系中乙酸甲酯的含量和乙醇含量的影响如图2所示。在300~600K范围内,乙酸甲酯的百分含量逐渐增大,而乙醇的百分含量逐渐减小的原因是____________。

(3)若压强为pkPa、温度为800K时,向2L恒容密闭容器中充入1molCH3OCH3和1molCO发生反应①,2min时达到平衡,则前2min内CH3COOCH3的平均生成速率为_________,该条件下平衡常数K=_____________。
(4)以铜为原料,利用电解法可制取具有广泛用途的光电材料——纳米Cu2O,其工作原理如图3所示。则b是_______极,电解时阳极的电极反应式为______________。

【答案】 2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g) △H=+116.0kJ/mol < < 300~600K范围内,随着温度升高,反应①对应的平衡体系向逆反应方向移动的程度比反应②的小 0.225mol·L-l·min-1 180 负 2Cu+2OH--2e-=Cu2O+H2O
【解析】(1)Cu2S与Cu2O反应生成Cu和SO2的化学方程式为Cu2S+2Cu2O=6Cu+SO2↑。由②×3-①,可得2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g) △H=+116.0kJ/mol。
(2)由图1可知,压强相同,温度升高,二甲醚和乙酸甲酯的平衡转化率均减小,则△H1和△H2都小于0,即△H1<0,△H2<0。温度升高,反应①和反应②均逆向移动,但反应②受温度影响更大,逆向移动程度大,导致乙酸甲酯的百分含量增大,乙醇的百分含量逐渐减小。
故答案为:<;< ;300~600K范围内,随着温度升高,反应①对应的平衡体系向逆反应方向移动的程度比反应②的小。
(3)由图1可知,压强为pkPa、温度为800K时,CH3OCH3的平衡转化率为0.9,根据已知条件,列出反应①的三段式:
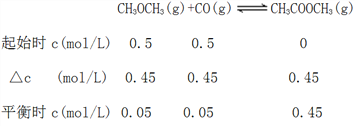
v(CH3COOCH3)=0.45mol/L÷2min=0.225mol·L-l·min-1;
K=![]() =180.
=180.
故答案为:0.225mol·L-l·min-1;180.
(4)电化学法制备Cu2O时,Cu失电子生成Cu2O,则Cu应为阳极,Fe为阴极。Fe接电源负极,则b为负极。电解时,阳极电极反应为2Cu+2OH--2e-=Cu2O+H2O。
故答案为:负;2Cu+2OH--2e-=Cu2O+H2O。


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:
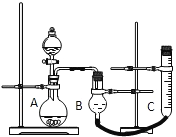
【题目】请用图中所示实验装置证明氧化铜能加快约7%的双氧水的分解并与二氧化锰的催化效果进行比较(即比较反应速率)。用图示装置测量产生气体的体积,其他可能影响实验的因素均已忽略,相关数据如下:
实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
① | 15mL | 无 | |
② | 15mL | CuO(0.5g) | |
③ | 15mL | MnO2(0.5g) |
(1)从实验原理来看,实验中的“待测数据”可以指___________,也可以指___________。
(2)实验时气体收集在B中,B仪器名称是___________。若要检验产生的气体是O2,待气体收集结束后,用弹簧夹夹住B下端乳胶管,打开单孔橡皮塞,___________。
(3)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验(不必写具体步骤):a.证明CuO的化学性质没有变化,b.______________。
(4)实验开始时,当往容器中加入一定量的双氧水后,由于短时间内产生大量气体,分液漏斗内的液体不能顺利流下,为了解决这个问题,你采取的措施是______________;在测量生成的气体体积时,除了要注意视线与凹液面相平以外,还应注意__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.聚甲基丙烯酸甲酯(PMMA)俗称有机玻璃。其结构简式为: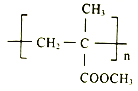 。以下是有机玻璃的一种合成路线:
。以下是有机玻璃的一种合成路线:
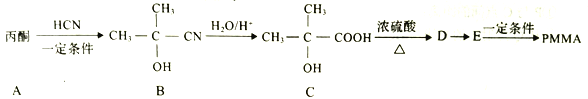
回答下列问题:
(1)A的结构简式为________,A生成B的反应类型是______反应。
(2)C中官能团的名称是________ ,D的名称是________(系统命名法)。
(3)由E生成PMMA的化学方程式为____________。
II.由合成PMMA得到的启示,可应用于由苯酚为主要原料制备![]()
(4)![]() 的同分异构体中符合下列条件的有_____种(不考虑立体异构):
的同分异构体中符合下列条件的有_____种(不考虑立体异构):
①属于![]() 的二取代物
的二取代物
②取代基处于对位且完全相同
③能够与NaHCO3溶液反应产生CO2
其中核磁共振氢谱有5个峰,峰面积之比为6:2:1:1的是_________(填结构简式)。
(5)参照I中有机玻璃的合成路线,设计并完善![]() 的合成路线:
的合成路线:
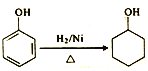 ____________
____________![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别加到HF溶液、CH3COOH溶液中,两混合溶液中离子浓度与pH的变化关系如图所示,已知pKa=-lgKa,下列有关叙述错误的是
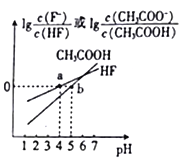
A. 常温下,Ka(CH3COOH)=10-5
B. a点时,c(F-)=c(HF)>c(Na+)>c(H+)>c(OH-)
C. 常温下,0.1mol/LNaF溶液的pH小于0.1mol/LCH3COONa溶液的pH
D. 向CH3COOH溶液中加入NaOH溶液后所得的混合溶液中, 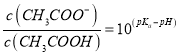
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是
A. H2SO4的摩尔质量是98
B. 等质量的O2和O3中所含的氧原子数相同
C. 等质量的CO与CO2中所含碳原子数之比为7︰11
D. 98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学--有机化学基础】有机物G(![]() )是一种调香香精,可用作抗氧剂,工业上合成它的路线图之一如下:
)是一种调香香精,可用作抗氧剂,工业上合成它的路线图之一如下:

(1)A中官能团的名称是_____,B→C的反应类型为_________。
(2)G分子中一定共平面的碳原子有______个。
(3)反应F→G中消耗的F与CH3MgBr的物质的量之比为______,B在浓硫酸存在下加热可通过一步反应得到E物质,但合成不采用此方法,其原因是__________。
(4)C→D的化学方程式为_______________。
(5)E有多种同分异构体,其中满足下列条件的同分异构体有_____种,写出核磁共振氢谱有4个吸收蜂的物质的结构简式:_______。
①含有一个六元环 ②1mol同分异构体与足量银氨溶液发生银镜反应生成4 mol Ag
(6)已知A转化为B的原理与F转化为G的相似,请设计以A为起始原料(其他试剂任选)制备![]() 的合成路线______________。
的合成路线______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述中一定正确的是
A. 1molFe与高温水蒸气反应,转移电子的数目为3NA
B. 标准状况下,2.24LHF中含有的极性键数目为0.1NA
C. 5mL0.1mol/LCH3COOH溶液和10mL0.5mol/LCH3COOH溶液中所含CH3COOH分子数相等
D. 一定条件下,向0.1L容器内通入4.6gNO2气体,NO2的物质的量浓度小于1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气有广泛用途,工业上利用反应N2(g)+3H2(g) ![]() 2NH3(g) H<0合成氨,其基本合成过程如下:
2NH3(g) H<0合成氨,其基本合成过程如下:
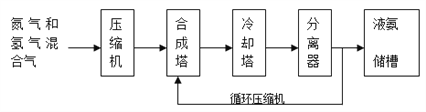
(1)某小组为了探究外界条件对反应的影响,以c0 mol/L H2参加合成氨反应,在a、b两种条件下分别达到平衡,如图A。
①a条件下,0~t0的平均反应速率v(N2)=___________mol·L-1·min-1。
②相对a而言,b可能改变的条件是______________________________。
③在a条件下t1时刻将容器体积压缩至原来的1/2,t2时刻重新建立平衡状态。请在答题卡相应位置画出t1~t2时刻c(H2)的变化曲线________。
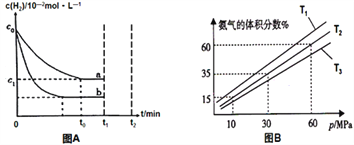
(2)某小组往一恒温恒压容器充入9 mol N2和23 mol H2模拟合成氨反应,图B为不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系图。若体系在T2、60MPa下达到平衡。
① 此时N2的平衡分压为__________MPa,H2的平衡分压为___________MPa。(分压=总压×物质的量分数)
② 列式计算此时的平衡常数Kp=____。(用平衡分压代替平衡浓度计算,结果保留2位有效数字)
(3)分离器中的过程对整个工业合成氨的意义是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧、得到CuO24.0g,若上述气体为NO和NO2的混合物,且体积比为1:2。则V可能为
A. 9.0 L B. 18.5L C. 25.7L D. 36.8L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com