
科目:高中化学 来源:不详 题型:单选题
| A.2.8g | B.5.6g | C.11.2g | D.1.4g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 mol | B.1.6 mol | C.2.2 mol | D.2.4 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
在空气中把铁灼烧至5000C就形成Fe3O4;温度再升高,可形成Fe2O3,在更高的温度下加热Fe2O3(约14000C)时,可失去氧,又得到Fe3O4。即: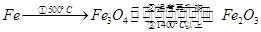 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:4 | B.2:7 | C.1:2 | D.3:8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H2O。
H2O。 kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是________kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)
kg的FeCO3,得到316.8 kg产品。若产品中杂质只有FeO,则该产品中Fe2O3的质量是________kg。(摩尔质量/g·mol-1:FeCO3 116 Fe2O3 160 FeO 72)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com