
分析 (1)由产物CO可知,SiO2与C化学计量数之比为1:2 由产物Si3N4可知SiO2与N2化学计量数之比为3:4,所以SiO2、C+、N2化学计量数之比为3:6:4,令SiO2的化学计量数为3,结合元素守恒可知Si3N4、CO化学计量数分别为1、6.
(2)反应中只有C元素的化合价升高,氮气有剩余,根据CO计算电子转移,C元素化合价由0价升高为+2价,转移电子的物质的量为CO的2倍.
(3)反应中N2作氧化剂,C是还原剂,N2将C氧化.
(4)由信息可知,氮化硅机械强度高,硬度大,热稳定性好,化学性质稳定,氮化硅属于原子晶体,不是电的良导体,制备氮化硅的资源丰富,自然界中有大量的氮气与二氧化硅,具有广阔的发展前景.
解答 解:(1)由产物CO可知,SiO2与C化学计量数之比为1:2 由产物Si3N4可知SiO2与N2化学计量数之比为3:2,所以SiO2、C、N2化学计量数之比为3:6:2,令SiO2的化学计量数为3,C、N2化学计量数分别为6、2,结合元素守恒可知Si3N4、CO化学计量数分别为1、6,配平后方程式为3SiO2+6C+2N2 $\frac{\underline{\;高温\;}}{\;}$ Si3N4+6CO.
故答案为:3、6、2、1、6;
(2)反应中只有C元素的化合价升高,氮气有剩余,根据CO计算电子转移,C元素化合价由0价升高为+2价,转移电子的物质的量为CO的2倍,所以反应中转移电子数为5mol×2×NAmol-1=10NA.
故答案为:10;
(3)反应中N2作氧化剂,C是还原剂,N2将C氧化为CO,所以氧化性C<N2,故答案为:<;
(4)A、氮化硅热稳定性好,可以用于热工设备,故A正确;
B、氮化硅属于原子晶体,不是电的良导体,故B错误;
C、氮化硅机械强度高,硬度大,可以替代同类型金属发动机,故C正确;
D、制备氮化硅的资源丰富,具有广阔的发展前景,故D错误.
故选:AC.
点评 本题考查氧化还原反应配平及计算、氧化性还原性比较、晶体结构与性质等,难度中等,注意掌握化学方程式常用的配平方法.


科目:高中化学 来源: 题型:选择题
| A. | 向氯化亚铁溶液中加入氢氧化钠溶液,先有白出现,后白色沉淀逐渐消失 | |
| B. | 将铜片放人氯化铁溶液,钢片表面生成银白色的铁 | |
| C. | 在氯化铁溶液中滴入氢氧化钠溶液,有红褐色沉淀出现 | |
| D. | 将铜粉加人冷的浓硝酸中会发生钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过NaOH溶液后再通过浓硫酸 | B. | 通过CuSO4溶液后再通过石灰水 | ||
| C. | 通过P2O5后再通过固体NaOH | D. | 通过碱石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
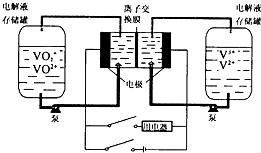
| A. | 充电时阴极的电极反应是V3++e-=V2+ | |
| B. | 放电时,VO2+作氧化剂,在正极被还原,V2+做还原剂,在负极被被氧化 | |
| C. | 若离子交换膜为质子交换膜,充电时当有1mol e-发生转移时,左槽电解液的H+的物质的量增加了1mol | |
| D. | 若离子交换膜为阴离子交换膜,放电时阴离子由左罐移向右罐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
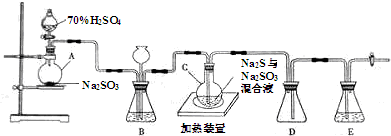
| 第一份 | 第二份 | 第三份 | |
| 样品的质量/g | 12.60 | 18.90 | 28.00 |
| 二氧化硫的体积/L | 1.12 | 1.68 | 2.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +2 | B. | +4 | C. | 0 | D. | +6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某无色溶液可能含有NH4+、Na+、Mg2+、Al3+、Fe3+、S042-、S032-、S2032-、C032一中的若干离子.为了探究其组成,分别取溶液100mL进行如下实验:
某无色溶液可能含有NH4+、Na+、Mg2+、Al3+、Fe3+、S042-、S032-、S2032-、C032一中的若干离子.为了探究其组成,分别取溶液100mL进行如下实验:| A. | 溶液中一定含有NH4+、C032- | |
| B. | 溶液中离子浓度c(Na+)=c(S042一) | |
| C. | 溶液中一定不含Mg2+、Al3+、Fe3+ | |
| D. | 溶液可能是由Na2C03与(NH4)2S04组成的混合溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
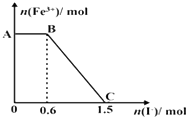
| A. | 图中AB段的氧化剂为K2Cr2O7 | |
| B. | 图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 | |
| C. | 开始加入的K2Cr2O7为0.25 mol | |
| D. | 若将上述过程中的KI溶液换为K3[Fe(CN)6]溶液,则有蓝色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com