
| A. | 鸡蛋清在水中形成的分散系是一种液溶胶,往其中加入饱和(NH4)2SO4溶液会生成白色沉淀 | |
| B. | 可用丁达尔效应来区分胶体和溶液 | |
| C. | 胶体中存在布朗运动,其他分散系中不存在布朗运动 | |
| D. | 某纯净纳米材料其粒子直径从几纳米到几十纳米,该纳米材料属于胶体 |
科目:高中化学 来源: 题型:选择题
| A. | 相同质量的水和冰相比较,冰的能量高 | |
| B. | 化学反应过程中能量的变化只有吸热和放热两种表现形式 | |
| C. | 化学反应既遵循质量守恒,也遵循能量守恒 | |
| D. | 需要加热才能发生的反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酸雨主要是空气中的SO2,溶于雨水中形成的 | |
| B. | 破坏臭氧层的主要物质是氟氯烃等物质 | |
| C. | 温室效应主要是因空气中CO2浓度增高造成的 | |
| D. | 居室装修释放的甲醛不会伤害人体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

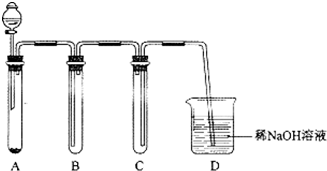
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
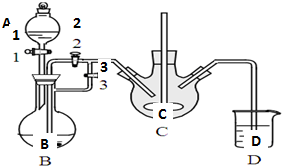 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,Mr=288)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化亚铁加入稀硝酸:FeO+2H+=Fe2++H2O | |
| B. | 硅酸钠水溶液中通入足量的二氧化碳:SiO32-+CO2+2H2O=H2SiO3(胶体)+CO32- | |
| C. | 碳酸氢铵溶液和足量氢氧化钠溶液混合:HCO3-+OH-=CO32-+H2O | |
| D. | 铝片加入烧碱溶液:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
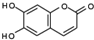 已知
已知 和NaOH 反应能生成RCOONa和R′OH,下列叙述正确的是( )
和NaOH 反应能生成RCOONa和R′OH,下列叙述正确的是( )| A. | M的相对分子质量是180 | |
| B. | 1mol M最多能与2molBr2发生反应 | |
| C. | 1molM与足量的NaOH溶液发生反应,所得有机产物的化学式为C9H4O5Na4 | |
| D. | 1molM与足量NaHCO3反应能生成2molCO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铍与铝原子核外具有相同的未成对电子数 | |
| B. | 氢氧化铍能与强酸、强碱溶液反应 | |
| C. | 铍与铝元素具有相同的最高正化合价 | |
| D. | 氧化铍只溶于强酸溶液,不溶于强碱溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com