
(12分)1.在探究铝和盐酸反应的实验现象是:“向铝片滴加盐酸,开始铝片表面出现少量气泡,而且气泡越来越多,甚至于使酸液 ‘沸腾’起来。”请解释上述现象。
 2.有同学设计了装置(见图),进行铝和盐酸反应制氢气的定量实验(铁架台等支垫仪器从略)。试回答下列有关问题
2.有同学设计了装置(见图),进行铝和盐酸反应制氢气的定量实验(铁架台等支垫仪器从略)。试回答下列有关问题
(1)装置中,导管的作用是:
(2)实验结束时,怎样测量实验中生成氢气的体积?
(3)实验中,准确测得4个数据:实验前锌粒的质量m1(g),实验后残留固体的质量m2(g),实验前、后量气管中液面读数分别为V1(mL)、V2(mL)。则通常情况时气体摩尔体积:![]()
1.铝片表面有一层氧化铝,故开始铝片表面露出少量氧化铝,与盐酸反应出现气泡较少;(1分)随后表面氧化铝溶解,露出金属铝越多,反应产生气泡越来越多;(1分)又因铝和稀硫酸反应放热,反应速率加快,故反应越来越剧烈(1分)
2.(1)使分液漏斗内气体压强与圆底烧瓶内气体压强相等。打开分液漏斗活塞时,盐酸能顺利流下(1分);滴入烧瓶的盐酸体积等于进入分液漏斗的体积,从而消除最初实验时加入盐酸引起的氢气体积误差。(1分)。
(2)实验结束,待装置冷却后,上、下移动漏斗,使漏斗内的液面与量气筒内的液面相平,在平视读取量气筒内的液面并读取体积数,即可推算反应产生的氢气在通常状况时的体积。(2分)。
(3)![]() V = 18(V1-V2)/ 1000(m1-m2) (L/mol)(2分 。
V = 18(V1-V2)/ 1000(m1-m2) (L/mol)(2分 。


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 |
| 4.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 反应结束 |
| 2.0mol/L硫酸 | 无明显现象 | 极少量气泡 | 少量气泡 | ||
| 4.0mol/L硫酸 | 无明显现象 | 少量气泡 | 有比较连续的气泡 | ||
 请回答:
请回答:| 实验目的 | 实验 编号 |
温度 | 金属铝 形态 |
盐酸浓度 /mol?L-1 |
| (1)实验①和②探究盐酸浓度对该反应速率的影响; (2)实验①和③探究温度对该反应速率的影响; (3)实验①和④探究金属规格(铝片、铝粉)对该反应速率的影响. |
① | 25?C | 铝片 | 4.0 |
| ② | 25?C 25?C |
铝片 铝片 |
2.0 2.0 | |
| ③ | 35℃ 35℃ |
铝片 铝片 |
4.0 4.0 | |
| ④ | 25?C 25?C |
铝粉 铝粉 |
4.0 4.0 |
| 1 |
| 2 |


查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
某探究小组同学用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速率的因素。
实验药品:2. 0moL/L盐酸、4. 0mol/L盐酸、2 .0mol/L硫酸、4.0mol/L硫酸,质量和相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50. 0mL,金属用量均为9. 0g。
(Ⅰ)甲同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 |
| 4.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 反应结束 |
| 2.0mol/L硫酸 | 无明显现象 | 极少量气泡 | 少量气泡 | ||
| 4.0mol/L硫酸 | 无明显现象 | 少量气泡 | 有比较连续的气泡 | ||
请回答:
(1)写出铝与盐酸反应的离子方程式 。
(2)反应1~15min内,铝与盐酸的反应速率逐渐加快,其原因是
。
(3)以上探究铝与稀盐酸、稀硫酸反应速率有差异,你认为其原因有哪些可能?请提出你的假设(说出2种可能): 。
(Ⅱ)(1)乙同学设计了如下影响反应速率因素的实验(温度控制为25℃和35℃)。请你根据实验目的帮助该同学完成以下实验设计表(用量:酸均为50. 0mL、铝为9. 0g过量):
| 实验目的 | 实验 编号 | 温度 | 金属铝 形态 | 盐酸浓度 /mol??L-1 |
| 1. 实验①和②探究盐酸浓度对该反应速率的影响; 2. 实验①和③探究温度对该反应速率的影响; 3. 实验①和④探究金属规格(铝片、铝粉)对该反应速率的影响。 | ① | 25??C | 铝片 | 4. 0 |
| ② | ||||
| ③ | ||||
| ④ |
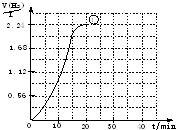
 (2)右图为实验①的“H2—t”曲线图,若
(2)右图为实验①的“H2—t”曲线图,若
上述反应浓度减少一倍,速率是原来的1/2;温
度每升高10 ℃,反速率是原来的2倍。请在
答题卡的座标中画出实验②和实验③的“H2—t”
曲线图。
查看答案和解析>>
科目:高中化学 来源:2009学年中山一中、翠园中学、宝安中学高三联考化学试题 题型:实验题
(13分)某探究小组同学用金属铝分别与稀盐酸或稀硫酸反应的方法研究金属与不同酸反应的差异及影响反应速率的因素。
实验药品:2. 0moL/L盐酸、4. 0mol/L盐酸、2 .0mol/L硫酸、4.0mol/L硫酸,质量和相同的铝片和铝粉(金属表面氧化膜都已除去);每次实验各种酸的用量均为50. 0mL,金属用量均为9. 0g。
(Ⅰ)甲同学用铝片分别和稀盐酸、稀硫酸反应,实验及其现象如下:
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 |
| 4.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 反应结束 |
| 2.0mol/L硫酸 | 无明显现象 | 极少量气泡 | 少量气泡 | ||
| 4.0mol/L硫酸 | 无明显现象 | 少量气泡 | 有比较连续的气泡 | ||
| 实验目的 | 实验 编号 | 温度 | 金属铝 形态 | 盐酸浓度 /mol?L-1 |
| 1. 实验①和②探究盐酸浓度对该反应速率的影响; 2. 实验①和③探究温度对该反应速率的影响; 3. 实验①和④探究金属规格(铝片、铝粉)对该反应速率的影响。 | ① | 25?C | 铝片 | 4. 0 |
| ② | | | | |
| ③ | | | | |
| ④ | | | |
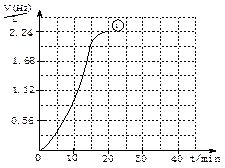 (2)右图为实验①的“H2—t”曲线图,若
(2)右图为实验①的“H2—t”曲线图,若查看答案和解析>>
科目:高中化学 来源:2009年广东省肇庆市高考化学一模试卷(解析版) 题型:解答题
| 反应进程(分钟) | 1 | 2 | 5 | 15 | 20 |
| 4.0mol/L盐酸 | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 反应结束 |
| 2.0mol/L硫酸 | 无明显现象 | 极少量气泡 | 少量气泡 | ||
| 4.0mol/L硫酸 | 无明显现象 | 少量气泡 | 有比较连续的气泡 | ||
| 实验目的 | 实验 编号 | 温度 | 金属铝 形态 | 盐酸浓度 /mol?L-1 |
| (1)实验①和②探究盐酸浓度对该反应速率的影响; (2)实验①和③探究温度对该反应速率的影响; (3)实验①和④探究金属规格(铝片、铝粉)对该反应速率的影响. | ① | 25?C | 铝片 | 4.0 |
| ② | ______ | ______ | ______ | |
| ③ | ______ | ______ | ______ | |
| ④ | ______ | ______ | ______ |
 ;温度每升高10℃,反速率是原来的2倍.请在答题卡的座标中画出实验②和实验③的“H2-t”曲线图______.
;温度每升高10℃,反速率是原来的2倍.请在答题卡的座标中画出实验②和实验③的“H2-t”曲线图______.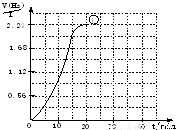
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com