
| I1/KJ·mol-1 | I2/KJ·mol-1 | I3/KJ·mol-1 | I4/KJ·mol-1 | I5/KJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |

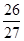 ×100%=96.3%,答案选C。
×100%=96.3%,答案选C。

科目:高中化学 来源:不详 题型:单选题
| A.Na、Mg、Al原子最外层电子数依次增多 |
| B.P、S、Cl元素最高正化合价依次增大 |
| C.N、O、F得电子能力依次减弱 |
| D.Li、Na、K的电子层数依次增多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 化学式 | 键长/nm | 键角 | 沸点/℃ |
| H2S | 1.34 | 92.3o | 一60.75 |
| H2Se | 1.47 | 91.0o | 一41.50 |
| 编号 | I5/kJ·mol-1 | I6/kJ·mol-1 | I7/kJ·mol-1 | I8/kJ·mol-1 |
| A | 6990 | 9220 | 11500 | 18770 |
| B | 6702 | 8745 | 15455 | 17820 |
| C | 5257 | 6641 | 12125 | 13860 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
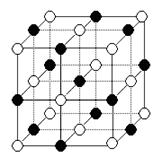
 键的数目为 。
键的数目为 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2O的熔点、沸点大于H2S的是由于H2O分子之间存在氢键。 |
| B.HF、HCl、HBr、HI的熔点沸点依次升高。 |
| C.乙醇分子与水分子之间只存在范德华力。 |
| D.氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.汗液中有AgNO3,可以与碘生成黄色沉淀 |
| B.汗液中有NaCl,可以与碘发生化学反应,有颜色变化 |
| C.根据相似相溶原理,碘易溶于皮肤分泌出的油脂中,有颜色变化 |
| D.根据相似相溶原理,碘与汗液中的淀粉有颜色变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com