
| 1.6g |
| 160g/mol |
| 10.44g |
| 174g/mol |
| 3.96g-0.02mol��56g/mol-0.04mol��39g/mol |
| 16g/mol |
| 1.6g |
| 160g/mol |
| 10.44g |
| 174g/mol |
| 3.96g-0.02mol��56g/mol-0.04mol��39g/mol |
| 16g/mol |
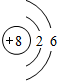 ���ʴ�Ϊ���������ڢ��壻
���ʴ�Ϊ���������ڢ��壻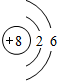 ��
��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K+ Na+ HSO3- NO3- |
| B��Mg2+ Al3+ SO42- OH- |
| C��K+ Fe2+ Cl- S2- |
| D��K+ Ba2+ NO3- SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.1mol/L Na2SO3��Һ�м�������NaOH���壬c��SO32-����c��Na+�������� |
| B��100��ʱ����pH=2��������pH=12��NaOH��Һ�������ϣ���Һ������ |
| C��25��ʱ��pH=5.6��CH3COOH��CH3COONa�����Һ�У�c��Na+����c��CH3COO-�� |
| D�������£�pH=1��������Һ������������c��H+����ˮ�������c��H+��֮��ֻΪ10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������¸�����Һ�������Ϊ��صĵ���� |
| B�������һ��ˮ��Һ�ʼ��� |
| C����C2H5NH3��NO3����NaOH��Ӧ����NH3 |
| D�������һ��ˮ������ӷ���ʽ���ʾΪ��C2H5NH3++H2O?C2H5NH2+H3O+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com