
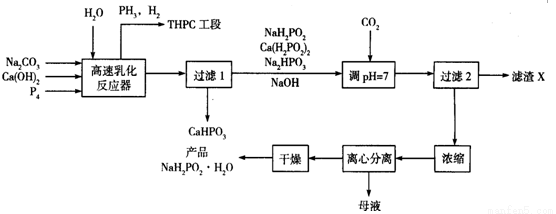
��ѧ������ָ��ʹ����ӵ���������������ԭ�����ڽ����Ƽ��ı����ϳ���һ�����ķ�������������(NaH2PO2)�ǻ�ѧ��������Ҫԭ�ϣ���ҵ���Ʊ�NaH2PO2��H2O���������£�
�ش���������:
�Ŵ�������(NaH2PO2)�Ǵ�����(H3PO2)������NaOH��Һ��Ӧ�IJ��NaH2PO2����_______(����Ρ�����ʽ�Ρ�����ʽ�Ρ����� NaH2PO2����Ԫ�صĻ��ϼ�Ϊ___________��
(2)�ڷ�Ӧ���м����黯�������ٽ����Ŀ����________________
(3)�ڷ�Ӧ���з��������Ӧ�����а���(P4)��Ca(OH)2��Ӧ���ɴ������Ƽ�����Ļ�ѧ����ʽΪ_________________________
(4)������ͨ��CO2��Ŀ����______________������X�Ļ�ѧʽΪ_____________
(5)������ĸҺ�е����ʳ�NaH2PO2�⣬���е�һ����Ҫ�ɷ�Ϊ_____________
(6)��PH3�ķ�������NaClO��NaOH�Ļ����Һ��������ת��Ϊ�����Σ��÷�Ӧ�����ӷ���ʽΪ____________
(7)ij������Ͷ���ԭ�ϰ���Ϊ1240 kg���ڸ����黯��Ӧ������80%�İ���ת��Ϊ�������Ƽ����⣬���������������ʧ�����������յõ���ƷNaH2PO2��H2O������ӦΪ__________kg(NaH2PO2��H2O����Է�������Ϊ106)

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡΫ���и�һ��ѧ�ڵ�һ���¿�ģ����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z�ֱ����3�ֲ�ͬ�Ķ�����Ԫ�أ�XԪ�ص�ԭ������������Ϊ1��YԪ��ԭ��M����6�����ӣ�ZԪ��ԭ�ӵ�L�������6����������Ԫ����ɵĻ�����Ļ�ѧʽ��
A. X3YZ4 B. X2YZ3 C. XYZ4 D. X4YZ4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�����и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���������ӻ����ﺬ���Ӽ���Ҳ���ܺ����Լ���Ǽ��Լ����ں�����Ԫ�صĻ����ﲻһ�������ӻ�������ɷǽ���Ԫ����ɵĻ�����һ���ǹ��ۻ����������״̬�ܵ���Ļ����������ӻ����������ȷ����
A. �ڢۢ� B. �٢ڢ�
C. �٢ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������ʡ���������ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�о�������Ⱦ��������ǻ�����һ����Ҫ����������Ӧ�úʹ������Ļ��������������������Ҫ���塣
��1����֪��N2��g��+O2��g��=2NO��g�� ��H=+180.5kJ•mol��1
2C��s��+O2��g��=2CO��g�� ��H=��221.0kJ•mol��1
C��s��+O2��g��=CO2��g�� ��H=��393. 5kJ•mol��1
������β�������ķ�Ӧ֮һ��2NO(g)+2CO(g)=N2(g)+2CO2(g)��H=_____ kJ•mol��1������
�÷�Ӧ�Է����е�������_______��ѡ����¡����¡�����

��2����0.20mol NO��0.10molCO����һ���ݻ��㶨Ϊ1L���ܱ������з�����Ӧ��
2NO��g��+2CO��g��?N2��g��+2CO2��g������Ӧ������ �������ʵ�Ũ�ȱ仯��ͼ��ʾ��
��Ӧ�ӿ�ʼ��9minʱ����CO2��ʾ�÷�Ӧ��������____________________������2λ��Ч���֣�
�ڵ�12minʱ�ı��������______________������»��¡�����
�۵�18minʱ�����µ�ƽ�⣬���¶��µ�ƽ�ⳣ��Ϊ______________���м���ʽ������24minʱ���������¶Ȳ��䣬���������г���CO��N2��0.060mol��ƽ�⽫_____�ƶ��������������������
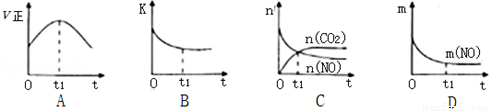
��3�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ��t1ʱ�̴ﵽƽ��״̬����________________������ţ���
����ͼ��v����K��n��m�ֱ��ʾ����Ӧ���ʡ�ƽ�ⳣ�������ʵ�����������
��4����Ϊȼ�Ͽ���������찱ȼ�ϵ�أ���������Ⱦ�����缫���Ͼ�Ϊ���Ե缫��KOH��Һ���������Һ����õ�ظ����缫��ӦʽΪ______________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������ʡ���������ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����װ��Ӧ����ʵ������NO����������ͭ��ʵ�飬�ܴﵽʵ��Ŀ���ǣ� ��
A. ��װ����ȡNO 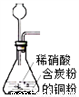 B. ��װ���ռ�NO
B. ��װ���ռ�NO 
C. ��װ�÷���̿�ۺ�����ͭ��Һ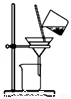 D. ��װ����������ͭ��Һ��Cu(NO3)2•3H2O
D. ��װ����������ͭ��Һ��Cu(NO3)2•3H2O 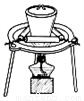
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017������ʡ��˳�и���3��ģ�⿼�������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
Ԫ��X��Y��Zԭ������֮��Ϊ36��X��Y��ͬһ���ڣ�X����Z2��������ͬ�ĺ�����Ӳ�ṹ�������Ʋⲻ��ȷ����
A. ͬ����Ԫ����X�Ľ�������ǿ
B. ԭ�Ӱ뾶X��Y�����Ӱ뾶X����Z2��
C. ͬ��Ԫ����Z���⻯���ȶ������
D. ͬ����Ԫ����Y����ۺ������������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ�����и����¸߿�ѡ����Ӧ�Կ��Ի�ѧ�Ծ��������棩 ���ͣ������
�Ȼ�李��״���������������Ҫ�����
��1����֪��
I NH4Cl(s)=NH3(g)+HCl(g) ��H=��l63.9 kJ��mol-1
II HCl(g)+CH3OH(g) CH3Cl(g)+H2O(g) ��H=-31.9kJ��mol-1
CH3Cl(g)+H2O(g) ��H=-31.9kJ��mol-1
III NH4Cl(s)+CH3OH(g) NH3(g)+CH3Cl(g)+H2O(g)
NH3(g)+CH3Cl(g)+H2O(g)
�� ��ӦIII��_________���������Է���Ӧ����ϸ��¶ȡ������ϵ��¶ȡ����κ��¶ȡ�����������_______________��
�� ͼ1�Ƿ�ӦIIIʹ�����ֲ�ͬ����ʱ�õ���CH3Cl�������¶ȹ�ϵ�ı仯ͼ��
��֪����������������������n(�״�)��n(�Ȼ��)��ֵ���״������ٶȡ���Ӧʱ��Ȳ�����������ͬ��
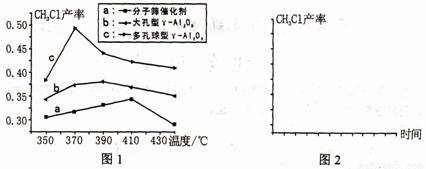
ͼ1 ��a����CH3Cl������������С��ԭ����___________������ͼ2�л���������������ͬʱ����370 ����ʹ�����ֲ�ͬ��������Ӧƽ��ʱ��CH3Cl�IJ�����ʱ���ϵ�ı仯���ߣ�����a��b��c�����Ӧ�����ߡ�_______________
��2��25 ��ʱ����ijŨ�ȵ�NH4Cl��Һ�еμ�һ�����İ�ˮ�����ԣ���ʱ�����Һ��c(Cl-)= 0.36mol �� L-1��������Һ��c (NH3 �� H2O)��_______mol �� L-1����25��ʱ��NH3��H2O��Kb=1.8��10-5��
��3�����Al2O3��Ĥ����Ϊ�������塢ģ��ϳ����ײ��ϵ���;�����Ըߴ���Ƭ��Ϊ�������������Ϊ������һ���ܶȵ�������Һ��Ϊ����ʽ��е�⣬���ɳ�����ȡ���Al2O3Ĥ����д������ȡ���̵������缫��Ӧ��__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ�����и����¸߿�ѡ����Ӧ�Կ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A. Zn��ϡH2SO4��Ӧ��2Zn+2H+=2Zn2++H2��
B. ������ˮ��Ӧ��Cl2+H2O=2H++Cl-+ClO-
C. ��Na2SiO3��Һ�еμ�ϡ���Na2SiO3+2H+=H2SiO3��+2Na+
D. ����������Һ���������������Һ��ϣ�H++SO42-+Ba2++OH-=BaSO4��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ�ĵ���У�߶���ѧ�ڵ�һ��������3�£���ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ� ��
A. ������,14g��ϩ�ͱ�ϩ�Ļ��������ԭ����Ϊ3NA��
B. 1mol����ϩ�к��е�̼̼˫����Ϊ4NA��
C. 17g�ǻ�����OH�������еĵ�������10 NA��
D. ����£�2.24L���к��е�̼ԭ����Ϊ0.6NA��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com