
【题目】设NA表示阿伏加德罗常数数值,下列叙述中正确的是( )
A.1.8 g的NH4+ 离子中含有的电子数为0.1NA
B.1mol Na2O2 固体中含离子总数为4NA
C.标准状况下,2.24L CCl4所含的共价键数为O.4NA
D.常温常压下,92g NO2和N2O4的混合气体含有的原子数为6NA
 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如图所示的微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
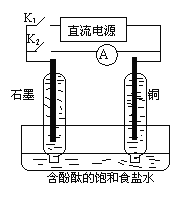
A. 断开K2,闭合K1时,总反应的离子方程式为:2H+ + 2Cl-![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为: Cl2+2e-=2Cl-
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的认识正确的是( )
A.油脂在空气中完全燃烧生成H2O和CO2
B.淀粉和纤维素互为同分异构体
C.金属钠可区分乙醇和乙酸
D.苯与饱和溴水混合,发生了取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A. NH3易液化,液氨常用作制冷剂
B. 稀HNO3氧化能力弱于浓HNO3
C. 贮存铵态氮肥时要密封保存,并放在阴凉处
D. 硝酸只能被ZnFe等金属还原成H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中是各组反应的反应物和反应温度,反应刚开始时放出H2速率最快的是( )
编号 | 金属(粉末状) | 酸的浓度及体积 | 反应温度 |
A | Mg,0.1 mol | 6mol·L-1硝酸10mL | 60℃ |
B | Mg,0.1 mol | 3mol·L-1盐酸10mL | 60℃ |
C | Fe,0.1 mol | 3mol·L-1L盐酸10mL | 60℃ |
D | Mg,0.1 mol | 3mol·L-1硫酸10mL | 60℃ |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组探究酸性条件下NO3-、SO42-、Fe3+三种微粒的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。(忽略氧气对反应的影响)
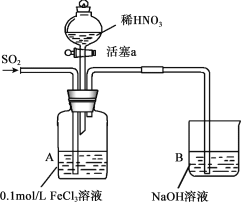
实验记录如下:
实验序号 | 实验操作 | 实验现象 |
I | 向A装置中通入一段时间的SO2气体。 | A中黄色溶液迅速变成深红棕色,最终变为浅绿色。 |
II | 取出少量A装置中的溶液,先加入KSCN溶液,再加入BaCl2溶液。 | 加入KSCN溶液后溶液不变色,再加入BaCl2溶液产生白色沉淀。 |
III | 打开活塞a,将过量稀HNO3加入装置A中,关闭活塞a | A中浅绿色溶液最终变为黄色。 |
IV | 取出少量A装置中的溶液,加入KSCN溶液;向A装置中通入空气。 | 溶液变为红色;液面上方有少量红棕色气体生成。 |
请回答下列问题:
(1)配制FeCl3溶液时,常常加入盐酸,目的是(用化学方程式和简单文字叙述): 。
(2)资料表明,Fe3+能与SO2结合形成深红棕色物质Fe(SO2)63+,反应方程式为: Fe3+ + 6SO2 ![]() Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
Fe(SO2)63+。请用化学平衡移动原理解释实验I中溶液颜色变化的原因 。
(3)实验II中发生反应的离子方程式是 。
(4)实验III中,浅绿色溶液变为黄色的原因是(用离子方程式表示) 。
(5)实验IV中液面上方有少量红棕色气体生成,发生反应的方程式是 。
(6)综合上述实验得出的结论是:在酸性条件下,NO3-、SO42-、Fe3+三种微粒的氧化性由强到弱的顺序是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl是海水中提取出来的一种重要物质,除可食用外,它还是一种重要的工业原料,下列以NaCl为原料的产品(或物质)是( )
① 烧碱 ② 纯碱 ③ 金属钠 ④ 氯气 ⑤ 盐酸 ⑥ NaClO
A.全部 B.①②③④⑤ C.①②③⑤⑥ D.①②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中不能用化合反应的方法制得的是
①SiO2 ②H2SiO3 ③Fe(OH)3 ④CuS ⑤FeCl2 ⑥ CaSiO3
A.②④ B. ②④⑤ C.②③④⑤ D.②④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com