
| A. | NaCl溶液 | B. | Ca(OH)2悬浊液 | C. | Fe(OH)3胶体 | D. | 油漆等乳浊液 |
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| B. | 用量筒量取20 mL 0.5000 mol•L-1H2SO4溶液于烧杯中,加水80mL配制成0.1000mol•L-1H2SO4溶液 | |
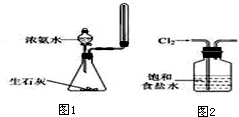
| C. | 实验室用图1所示装置制取少量氨气 | |
| D. | 实验室用图2所示装置除去Cl2中的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体密度不再发生变化 | |
| B. | A的物质的量浓度不再改变 | |
| C. | 容器内总压强不再改变 | |
| D. | 单位时间内消耗4nmolA,同时消耗5nmolB |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60mL 1mol•L-1氯化钠溶液 | B. | 75mL 1mol•L-1氯化钙溶液 | ||
| C. | 60mL 3mol•L-1氯化钾溶液 | D. | 75mL 1.5mol•L-1氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
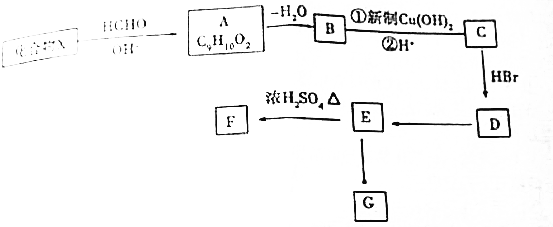
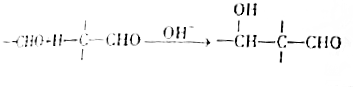
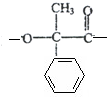
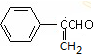 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$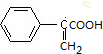 +Cu2O+2H2O
+Cu2O+2H2O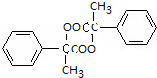
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
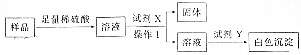

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知:0.4mol液态N2H4与足量的液体双氧水反应,生成氮气和水蒸气,放出200.0kJ的热量.
已知:0.4mol液态N2H4与足量的液体双氧水反应,生成氮气和水蒸气,放出200.0kJ的热量.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、K+、Cl-、HCO3- | B. | K+、Ba2+、OH-、NO3- | ||
| C. | Mg2+、Cu2+、Cl-、SO42- | D. | Na+、Cl-、Ba2+、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
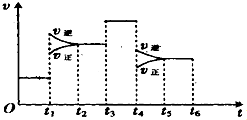 在一密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图表示该反应的速率(v)在某一时间段内的变化.则下列时间段中,SO3的百分含量最高的是( )
在一密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,如图表示该反应的速率(v)在某一时间段内的变化.则下列时间段中,SO3的百分含量最高的是( )| A. | t0→t1 | B. | t2→t3 | C. | t3→t4 | D. | t3→t5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com