
在2A+B⇌3C+4D反应中,表示该反应速率最快的是()
A. υ(A)=0.5 mol/(L•s) B. υ(B)=1 mol/(L•s)
C. υ(C)=0.8 mol/(L•s) D. υ(D)=0.3 mol/(L•s)
考点: 反应速率的定量表示方法.
专题: 化学反应速率专题.
分析: 利用速率之比等于化学计量数之比转化为用同一物质表示的速率,然后再进行比较.
解答: 解:都转化为D物质表示的速率进行比较,对于2A+B⇌3C+4D,
A、υ(A)=0.5 mol/(L•s),速率之比等于化学计量数之比,故υ(D)=2υ(A)=1mol/(L•s),
B、υ(B)=1mol/(L•s),速率之比等于化学计量数之比,故υ(D)=4υ(B)=4mol/(L•s),
C、υ(C)=0.8mol/(L•s),速率之比等于化学计量数之比,故υ(D)=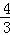 υ(C)=
υ(C)=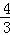 ×0.8mol/(L•s)=1.1mol/(L•s),
×0.8mol/(L•s)=1.1mol/(L•s),
D、υ(D)=0.3 mol/(L•s),
故速率B>C>A>D,
故选B.
点评: 本题考查反应速率快慢的比较,难度不大,注意比较常用方法有:1、归一法,即按速率之比等于化学计量数之比转化为用同一物质表示的速率,2、比值法,即由某物质表示的速率与该物质的化学计量数之比,比值越大,速率越快.


科目:高中化学 来源: 题型:
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)═2C(g),反应2min的时间,并测得该段时间内C的反应速率为0.6mol•L﹣1•min﹣1,现有下列几种说法中正确的是()
①用物质A表示的反应的平均速率为0.6mol•L﹣1•s﹣1
②用物质B表示的反应的平均速率为0.05mol•L﹣1•s﹣1
③2min时容器中A的物质的量为2.8mol
④2min时物质B的浓度为0.4mol•L﹣1.
A. ①③ B. ②④ C. ②③ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
依据事实,写出下列反应的热化学方程式.
(1)已知拆开1mol H﹣H键,1mol N﹣H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为: .
(2)以甲烷为原料制取氢气是工业上常用的制氢方法.
已知:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.2kJ•mol﹣1
CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=+247.4kJ•mol﹣1
请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学反应速率的说法中,正确的是()
A. 100mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
B. 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
C. 二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速率减慢
D. 汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个容积为VL的密闭容器中放入2LA(g)和1L B(g),在一定条件下发生下列反应:3A(g)+B(g)⇌nC(g)+2D(g),达到平衡后,A物质的量浓度减小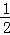 ,混合气体的平均摩尔质量增大
,混合气体的平均摩尔质量增大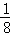 ,则该反应的化学方程式中n的值是()
,则该反应的化学方程式中n的值是()
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
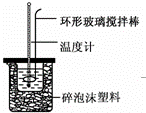
实验室用50mL 0.50mol•L﹣1盐酸、50mL 0.55mol•L﹣1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
实验次数 起始温度t1/℃ 终止温度t2/℃
盐酸 NaOH溶液
1 20.2 20.3 23.7
2 20.3 20.5 23 .8
.8
3 21.5 21.6 24.9
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是 .
(2)在操作正确的前提下,提高中和热测定准确性的关键是: .
(3)根据上表中所测数据进行计算,则该实验测得的中和热△H= .如用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将 (填“偏大”、“偏小”、“不变”).
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温 较高
较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学科学的叙述中,正确的是()
A. 化学学科与其他学科分支的联系不紧密
B. 化学知识只是在工业生产中起到重要作用
C. 化学研究会造成严重的环境污染,最终人类将毁灭在化学物质中
D. 化学科学是在原子、分子水平上研究物质的组成、结构、性质、变化、制备和应用的重要自然科学
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
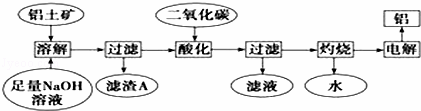
已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的Na2SiO3与Na2与 反应,能生成硅铝酸盐沉淀,化学反应方程式为:
反应,能生成硅铝酸盐沉淀,化学反应方程式为:
2Na2SiO3+2Na2═2Na2Al2Si2O8↓+2H2O+4NaOH
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中主要发生反应的离子方程式: ; .
(2)滤渣A的主要成分为 ;滤渣A的用途是(只写一种) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com