
| J | ||||
| R |
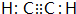 .
.| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入氧气 | 加入乙的物质 |
| y | 乙的物质的量 | 平衡常数K | 乙的转化率 | 生成物物质的量总和 |
分析 J、L、M、R、T是原子序数依次增大的短周期主族元素,由元素在周期表中的位置可知,J处于第二周期,R处于第三周期,J元素最低负化合价的绝对值与其原子最外层电子数相等,故J原子最外层电子数为4,故J为碳元素,则R为硫元素,T的原子序数最大,故T为Cl元素,M是地壳中含量最多的金属元素,则M为Al,由(4)中L的最简单气态氢化物丙的水溶液显碱性,则L为氮元素,丙为NH3,据此解答.
解答 解:J、L、M、R、T是原子序数依次增大的短周期主族元素,由元素在周期表中的位置可知,J处于第二周期,R处于第三周期,J元素最低负化合价的绝对值与其原子最外层电子数相等,故J原子最外层电子数为4,故J为碳元素,则R为硫元素,T的原子序数最大,故T为Cl元素,M是地壳中含量最多的金属元素,则M为Al,由(4)中L的最简单气态氢化物丙的水溶液显碱性,则L为氮元素,丙为NH3.
(1)T为Cl元素,处于周期表中第三周期第ⅦA族,故答案为:第三周期第ⅦA族;
(2)化合物甲的分子由两个C原子和两个氢原子构成,则甲为C2H2,电子式是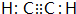 ,故答案为:
,故答案为: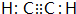 ;
;
(3)R元素的最高价氧化物乙为SO3,发生分解反应:2SO3?2SO2+O2 △H>0,
a.该反应是吸热反应,温度升高,平衡向正反应移动,SO3的物质的量减小,故a符合;
b.化学平衡常数只受温度影响,温度升高,平衡向正反应移动,平衡常数增大,故b不符合;
c.加入O2的物质的量,氧气的浓度增大,平衡向逆反应进行,SO3的转化率降低,故c符合;
d.加入SO3的物质的量,平衡向正反应进行,总的物质的量增大,故d不符合;
故答案为:ac;
(4)L的最简单气态氢化物丙的水溶液显碱性,则L为氮元素,丙为NH3,丙的水溶液可作H2O2的清除剂,反应的产物不污染环境,应生成氮气与水,其化学方程式为:NH3+3H2O2=N2+6H2O,故答案为:NH3+3H2O2=N2+6H2O;
(5)在298K下,根据C、Al各1mol完全燃烧,分别放出热量以a kJ和b kJ时,可得热化学方程式:
①4Al(s)+3O2(g)=2Al2O3(s),△H=-4bkJ/mol,
②C(s)+O2(g)=CO2(g),△H=-akJ/mol,
根据盖斯定律,将①-②×3得铝与二氧化碳发生置换反应的热化学方程式为4Al(s)+3CO2(g)=3C(s)+2Al2O3(s)△H=(+3a-4b)kJ/mol,
故答案为:4Al(s)+3CO2(g)=3C(s)+2Al2O3(s)△H=(+3a-4b)kJ/mol;
(6)用铝作阳极,碳单质作阴极,Ca(HC03)2溶液作电解液,进行电解,阴极氢离子放电产生氢气,同时有氢氧根离子产生,将碳酸氢根变成碳酸根,结合钙离子生成碳酸钙沉淀,阳极为铝放电,生成铝离子,铝离子与碳酸氢根离子双水解生成二氧化碳气体和氢氧化铝沉淀,阳极电极反应式为Al-3e-+3HCO3-=Al(OH)3+3CO2↑,
故答案为:H2、CaCO3;Al-3e-+3HCO3-=Al(OH)3+3CO2↑.
点评 本题考查元素周期表、常用化学用语、影响化学平衡的因素、热化学方程式书写、原电池等,题目较为综合,难度中等,注意对基础知识的全面理解掌握,推断元素是关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | CH3COOH电离程度变大 | B. | 溶液pH变大 | ||
| C. | 溶液中c(H+)减小 | D. | 溶液的导电能力减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 利用图1除去Cl2中的HCl | |
| B. | 利用图2由45°白酒制无水乙醇 | |
| C. | 利用图3检验产物中含有乙烯 | |
| D. | 图4是研究温度对NO2和N2O4平衡的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )
已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )| A. | a条件下的反应速率小于b条件下的反应速率 | |
| B. | 其他条件相同时,a表示有催化剂,b表示无催化剂 | |
| C. | 其他条件相同,若a、b表示不同压强下的反应,则n>2 | |
| D. | 其他条件相同,若a、b表示不同温度下的反应,则x>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

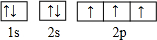 ,这样排布遵循了构造原理、泡利原理和洪特规则.
,这样排布遵循了构造原理、泡利原理和洪特规则.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 :下列有关该化合物的说法中正确的是( )
:下列有关该化合物的说法中正确的是( )| A. | 分子式为C12H8O2Cl4 | B. | 是一种可溶于水的气体 | ||
| C. | 是最危险的致癌物之一 | D. | 是一种多卤代烃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com