
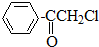


 与氢气发生加成反应生成A(
与氢气发生加成反应生成A( ),在浓硫酸、加热条件下发生消去反应生成B(
),在浓硫酸、加热条件下发生消去反应生成B( ),与溴发生加成反应生成C(
),与溴发生加成反应生成C( ),在发生水解反应生成D(
),在发生水解反应生成D( ),最后发生氧化生成
),最后发生氧化生成 ,以此解答.
,以此解答. ,
, ;
; 与氢气发生加成反应生成A(
与氢气发生加成反应生成A( ),在浓硫酸、加热条件下发生消去反应生成B(
),在浓硫酸、加热条件下发生消去反应生成B( ),与溴发生加成反应生成C(
),与溴发生加成反应生成C( ),在发生水解反应生成D(
),在发生水解反应生成D( ),最后发生氧化生成
),最后发生氧化生成 ,
,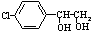 ,故答案为:H2;
,故答案为:H2;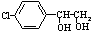 ;
;
| 浓硫酸 |
| △ |
 +H2O,
+H2O,
| 浓硫酸 |
| △ |
 +H2O.
+H2O.


科目:高中化学 来源: 题型:
| 元素A | 元素B | 元素C | 元素X | 元素Y | 元素Z |
| 单质是一种常见金属,与元 素X形成黑色和红棕色三种常见化合物 |
单质是一种黄绿色气体 | 短周期中金属性最强,与X 反应能生成两种常见化合物 |
最外层电子数是内层电子数的3倍,能形 成双原子阴离子 |
单质为双原子分子,结构中б键与π键数 目比为1:2 |
阳离子就是一个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | Al | B | Be | C | Cl | F | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电流方向:电极Ⅳ→A→电极Ⅰ |
| B、电极Ⅰ发生还原反应 |
| C、电极Ⅱ逐渐溶解 |
| D、电极Ⅲ的电极反应:Cu2++2e-═Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | Ⅰ | Ⅱ | Ⅲ |
| A | 稀氨水 | Al3- | Mg2- |
| B | 稀硝酸、AgNO3溶液 | Cl- | I- |
| C | KSCN溶液 | Fe2+ | Fe3+ |
| D | 稀盐酸、BaCl2溶液 | SO42- | SO32- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com