


科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
C、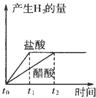 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用10 mL 量筒量取5.2 mL盐酸 |
| B、向小试管中加入100mL稀盐酸 |
| C、用托盘天平称取25.12gNaCl固体 |
| D、用100 mL容量瓶配制50mL0.1 mol/L的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
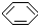 来表示,下列关于苯的叙述中正确的是( )
来表示,下列关于苯的叙述中正确的是( )| A、苯主要是以石油为原料而获得的一种重要化工原料 |
| B、苯中含有碳碳双键,所以苯属于烯烃 |
| C、分子中的6个碳碳化学键完全相同 |
| D、苯可以使高锰酸钾溶液反应褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述反应是复分解反应 |
| B、产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成磷酸小液滴(雾) |
| C、因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替 |
| D、上述反应中消耗3molP时,转移电子的物质的量为30mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、50 mL 12 mol?L-1 浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| B、5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C、5g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA |
| D、常温常压下,46g NO2与N2O4的混合气体中含有的原子总数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com