
����Ŀ���ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJmol��1��ʾ��������۲���ͼ��Ȼ��ش����⣮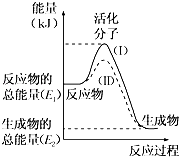
��1��ͼ����ʾ��Ӧ��������ȡ����ȡ�����Ӧ��
��2����֪��1mol H��H����1molI��I��1mol H��I���ֱ���Ҫ���յ�����Ϊ436kJ��151kJ��299kJ������1mol������1mol�ⷴӦ����HI������ų��������ա��� kJ���������ڻ�ѧ��Ӧ�����У��ǽ�ת��Ϊ ��
��3�����з�Ӧ�У����ڷ��ȷ�Ӧ���� �� �������ȷ�Ӧ���� ��
������ȼ�ա� ��ըҩ��ը�� ������кͷ�Ӧ�� �ܶ�����̼ͨ�����ȵ�̼
��Ba��OH��28H2O��NH4Cl��Ӧ ��������ϡ���ᷴӦ��
���𰸡�
��1������
��2���ų���11����ѧ�ܣ�����
��3���٢ڢۢޣ��ܢ�
���������⣺��1������ͼ�������Ӧ��������������������������Ӧ���ȣ����Դ��ǣ����ȣ���2���ڷ�ӦH2+I22HI�У�����1molH��H����1molI��I�������յ�����Ϊ��1��436kJ+151kJ=587kJ������2molHI�����γ�2molH��I�����ų�������Ϊ��2��299kJ=598kJ�����յ������٣��ų��������࣬���Ը÷�ӦΪ���ȷ�Ӧ���ų�������Ϊ��598kJ��587kJ=11kJ����ѧ��ת��Ϊ���ܣ����Դ��ǣ��ų���11����ѧ�ܣ����ܣ���3�������ķ��ȷ�Ӧ�У����е�����ȼ�ա����н������ᷴӦ��������ˮ��Ӧ�������кͷ�Ӧ������������Ϸ�Ӧ�����ȷ�Ӧ�����������ȷ�Ӧ�У��������ֽⷴӦ������Ļ��Ϸ�Ӧ����C��CO2����ijЩ���ֽ⣨����κ�ǿ������Է��ȷ�Ӧ�У��٢ڢۢޣ����ȷ�Ӧ�У��ܢݣ�
���Դ��ǣ��٢ڢۢޣ��ܢݣ�
�����㾫�������ڱ��⿼��ķ�Ӧ�Ⱥ��ʱ䣬��Ҫ�˽��ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�Ȳ��ܵó���ȷ�𰸣�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ����������ϸ���ں������٣���ȴ����������ɻ�ȱ���ǣ� ��
A. C��H��N��P��Mn
B. Cl��Fe��S��N��Mg
C. B��Cu��Zn��Mn��Mo
D. N��P��K��Cu��Fe��I
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���Ĺ�ҵ�Ʒ�������ǣ� ��
A.��ϩ����������ȩB.��ˮ���������ʯ�ҹ����Ƽ���
C.ʯ���ѻ�������D.ú�����Ʊ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϴ�������˵���㲻����!����1902��10��24 �µ�����ѧ������˹��ʩ�ᷢ����������Ҳֻ�ж̶̵�һ�ٶ���ʱ�䣮��Щ�������̡����СС�����ϴ��������ƻ����о��ۣ��Ի�����Σ��Ҳ�Ǽ����˵ģ�2008��6��1���𣬸��ݹ���ԺҪ�����г��С��̳�����ó�г�����Ʒ���۳���ʵ�����Ϲ�����г�ʹ�ã�����˵����ȷ���ǣ� ��
A.�۱�ϩ���ϵĽṹ��ʽΪ ![]()
B.������ϩ���ϵ���ĵ���ʽΪ ![]()
C.���Ϲ����������ԭ����Ҫ���Ĵ���ľ��
D.����ϩ�к�̼�����������䵥��ĺ�̼����������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ�У�PΪһ�����ɻ����Ļ������ر�K���ֱ�������A��B�и�����1mol X��1mol Y����ʼʱ��VA=a L��VB=0.8a L����ͨ�ܵ�������Բ��ƣ�������ͬ�¶Ⱥ��д������ڵ������£��������и��Է���������Ӧ��3X��g��+3Y��g��2Z��g��+2W��g������ƽ��ʱ��VB=0.6a L���ش��������⣺ 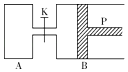
��1���ﵽƽ��ʱB��X��ת����Ϊ ��
��2��ƽ��ʱA��B�л�������ƽ����Է��������Ĺ�ϵ�ǣ�MAMB�����������=����������
��3����K��һ��ʱ���Ӧ�ٴδﵽƽ�⣬��B�����ΪL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ҩ���ƣ�Tamiflu������ç���ᣨA��Ϊԭ�ϣ�����ʮ����Ӧ�ϳ��Ƶã�ç������Դӳ��õ�������ϡ��˽ǡ�����ȡ����Ƽ�A��ç���ᣩ��B�Ľṹ��ʽ��ͼ�ף�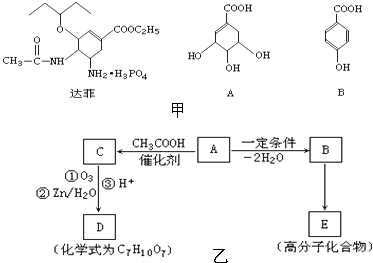
��֪�� ![]()
������A��B��C��D������ͼ����ʾ��ת����ϵ��
�ش��������⣺
��1��д������к��������ŵ����ƣ���
��2��д��A��C�ķ�Ӧ���ͣ���
��3��д��B��E�Ļ�ѧ����ʽ����
��4��д��D�Ľṹ��ʽ����
��5����֪B�ж���ͬ���칹�壬д��һ�ַ����������ʵ�B��ͬ���칹��Ľṹ��ʽ����FeCl3��Һ��������ɫ��
��������Cu��OH��2����Һ���ò�����ɫ������
�۱����ϵ�һ±������2�֣�
��6�����A����C��Ŀ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.��NaAlO2��Һͨ�������CO2��2AlO ![]() +CO2+3H2O�T2Al��OH��3��+CO
+CO2+3H2O�T2Al��OH��3��+CO ![]()
B.������������Fe3O4����������Fe3O4+2I��+8H+�T3Fe2++I2+4H2O
C.��FeS��ȥ��ҵ��ˮ�е�Hg2+��Hg2++S2���THgS��
D.�͵�Ca��OH��2��Һ�еμӹ���NaHCO3��Һ��HCO ![]() +Ca2++OH���TCaCO3��+H2O
+Ca2++OH���TCaCO3��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���к��ȵIJⶨʵ�飨��ͼ���� 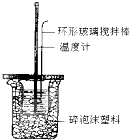
����ȡ��Ӧ��ʱ��ȡ50mL0.50molL��1�����ᣬ��Ӧ������Լ���������ţ���
A��50mL0.50molL��1NaOH��Һ
B��50mL0.55molL��1NaOH��Һ
C��1.0gNaOH����
���ڸ�ʵ������У���ͬѧ��Ҫ�ⶨ��ʵ��������������ţ���
A�������Ũ�� B��������¶�
C������������Һ��Ũ�� D������������Һ���¶�
E��ˮ�ı����� F����Ӧ������Һ����ֹ�¶�
������50mL0.5molL��1������Һ������������ⶨ�к��ȣ��������� �� ���ƫ��ƫС�����䡱��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ͻ��������Ϻ���ij�ְ�ɫǦ������������ڿ����г�ʱ���ͻ��ɺ�ɫPbS���Ӷ�ʹ�ͻ���ɫ�ʱ䰵������˫��ˮH2O2����ϴ����ɽ�PbS���PbSO4���Ӷ�ʹ�ͻ���ԭ��������ϴ��Ӧ�Ļ�ѧ����ʽΪ PbS+ 4H2O2 = PbSO4 + 4M������ƽ��
��1��������M�Ļ�ѧʽΪ_________________________
��2���ڴ˷�Ӧ�У�PbS�� _____________����H2O2�� _____________��
��3��������ת�Ƶĵ�����Ŀ2molʱ���μӷ�Ӧ��H2O2������Ϊ ___________ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com