
| A. | A2B | B. | AB2 | C. | AB3 | D. | A2B5 |
科目:高中化学 来源: 题型:选择题
| A. | 苯酚钠溶液中通入少量二氧化碳:2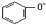 +2H2O+CO2→2 +2H2O+CO2→2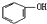 +CO32- +CO32- | |
| B. | 等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| C. | 向AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 同位素示踪法可用于反应机理的研究:2KMnO4+5H218O2+3H2SO4═K2SO4+2MnSO4+518O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
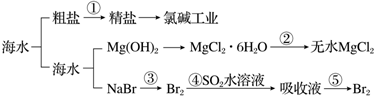
| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液-→NaOH溶液-→BaCl2溶液-→过滤后加盐酸 | |
| B. | 工业上金属钠是通过氯碱工业制取 | |
| C. | 从第③步到第⑤步的目的是为了富集溴元素 | |
| D. | 在第③④⑤步中溴元素均被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5amol | B. | 0.1amol | C. | 0.1+amol | D. | 2amol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
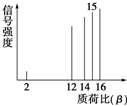 质谱法能够对有机分子进行结构分析.其方法是让极少量的(10-9 g)化合物通过质谱仪的离子化室,样品分子大量离子化,少量分子碎裂成更小的离子,然后测定其质荷比.其有机物样品的质荷比如图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),该有机物可能是( )
质谱法能够对有机分子进行结构分析.其方法是让极少量的(10-9 g)化合物通过质谱仪的离子化室,样品分子大量离子化,少量分子碎裂成更小的离子,然后测定其质荷比.其有机物样品的质荷比如图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),该有机物可能是( )| A. | 甲醇(CH3OH) | B. | 甲烷 | C. | 丙烷 | D. | 乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com