碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.
(1)使Cl
2和H
2O(g)通过灼热的炭层,生成HCl和CO
2,当有1molCl
2参与反应时释放出145KJ热量,写出该反应的热化学方程式
2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0kJ?mol-1
2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290.0kJ?mol-1
(2)科学家利用太阳能分解水生成的氢气在催化剂作用下与CO
2反应生成甲醇.已知H
2(g)、CO(g)和CH
3OH(l)的燃烧热分别为285.8KJ/mol
-1、283.0kJ?mol
-1和726.5kJ?mol
-1.则:①利用太阳能分解10mol水消耗的能量是
2858
2858
kJ.
②甲醇不完全燃烧生成CO和液态水的热化学方程式为
CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-443.5kJ?mol-1
CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-443.5kJ?mol-1
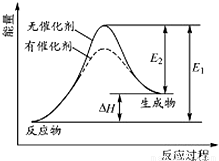
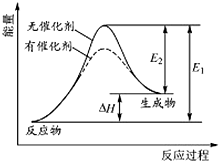
(3)某反应的反应过程中能量变化如图 所示(图中E
1 表示正反应的活化能,E
2 表示逆反应的活化能).下列有关叙述正确的是
ACD
ACD
A.该反应为吸热热反应
B.催化剂能改变该反应的焓变
C.催化剂能降低该反应的活化能
D.逆反应的活化能小于正反应的活化能.

 碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.
碳是化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质.