
| A�� | MԪ��λ�����ڱ��еĵ������ڵ�VIA�� | |
| B�� | ZԪ���ǹ裬������Ȼ���д�������̬ | |
| C�� | X��M�ĵ����ڸ����·�Ӧ�õ��Ķ�Ԫ����������У����ڼ��Թ��ۼ� | |
| D�� | ����Ԫ���е�Y���ʿ����ں��պ���Ͻ���ϵ��Ʊ� |
���� ������Ԫ��X��Y��Z��M��ԭ��������������Ԫ��X��һ�ָ�Ӳ�ȵ����DZ�ʯ����XΪCԪ�أ�Y2+���Ӳ�ṹ������ͬ����YΪMg��Z��������Ϊż����������M����Ϊ����ɫ���壬��ZΪSi��MΪSԪ�أ�Ȼ����Ԫ�ػ�����֪ʶ�����
��� �⣺������Ԫ��X��Y��Z��M��ԭ��������������Ԫ��X��һ�ָ�Ӳ�ȵ����DZ�ʯ����XΪCԪ�أ�Y2+���Ӳ�ṹ������ͬ����YΪMg��Z��������Ϊż����������M����Ϊ����ɫ���壬��ZΪSi��MΪSԪ�أ�
A��MΪSԪ�أ�������������Ϊ2��8��6����3�����Ӳ㣬����������Ϊ6���ʴ��ڵ�������VIA�壬��A��ȷ��
B��ZԪ����Si��Ϊ����Ԫ�أ��Ի���̬���ڣ���B����
C��X̼����ĵ����ڸ����·�Ӧ����CS2����Ӧ��ѧ����ʽΪC+2S$\frac{\underline{\;����\;}}{\;}$CS2���������Ϊֱ���Σ��ṹ�������̼���ƣ��������ɲ�ͬԪ��ԭ���γɵĹ��ۼ����仯ѧ�����ڼ��Թ��ۼ�����C��ȷ��
D������Ԫ����ֻ��MgΪ����Ԫ�أ��ܶȱȽ�С���ƳɵĺϽ�Ӳ�ȴ����ں��պ���Ͻ���ϵ��Ʊ�����D��ȷ��
��ѡB��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ɣ�Ϊ��Ƶ���㣬����ԭ�ӽṹ��Ԫ�ػ�����֪ʶ�ƶ�Ԫ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�ػ������Ӧ�ã���Ŀ�ѶȲ���


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���������ɫ���壬������ͨ�����ʯ��ˮ�У���Һ����ǣ�һ����CO32- | |
| B�� | �����Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��һ����SO42- | |
| C�� | ���������ữ�����ᱵ��Һ������Ҳ���������ɣ��ټ���������Һ�������ְ�ɫ������һ����Cl- | |
| D�� | ����̼������Һ������ɫ�������ټ������ɫ������ʧ��һ����Ca2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
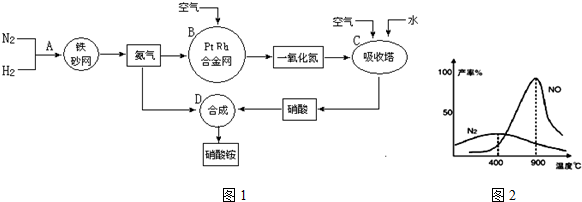
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����£�22.4L������ȫ����ˮת�Ƶ�����ΪNA | |
| B�� | 32gS��ȫ��������������Һת�Ƶ�����Ϊ2 NA | |
| C�� | ����£�6.72LNO2��ȫ����ˮת�Ƶ�����ΪNA | |
| D�� | 28.8g������ͭ����ϡ����ת�Ƶ�����Ϊ0.2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֤ij�л�������������ɵ�ʵ��ֻҪ֤������ȫȼ�պ�IJ���ֻ��H2O��CO2 | |
| B�� | ú����õ���ú���Ϳ��Է��������������ɫ��ζ��Һ̬�� | |
| C�� | �ƾ��д��ڵ�ijЩ�������ʹ�����Ҵ�������ת��Ϊ���ᣬ�ƾ�������ζ | |
| D�� | ��ϩʹ���Ը��������Һ��������Ȼ�̼��Һ��ɫ��������ϩ�����˼ӳɷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �٢ڢۢ� | C�� | �ڢۢݢ� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��չ̫���ܷ��硢����CO2����ȫ�������϶�����Ч���ٻ�����Ⱦ | |
| B�� | ũҵ��������й�ҵ�л������P�������ж��̲��ŷḻ���������� | |
| C�� | ú�ĸ����ǽ�ú����������ǿ�ȣ��õ���̿��ú���͡���¯���� | |
| D�� | ʯ�Ͳ�Ʒ�������ھۺϷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com