
【题目】(题文)常温下,某水溶液M中存在的离子有Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A。根据题意回答下列问题:
(1)写出酸H2A的电离方程式_________________________。
(2)若溶液M由10 mL 2 mol·L-1NaHA溶液与10 mL 2 mol·L-1 NaOH溶液等体积混合而成,则溶液M的pH________(填“<”“>”或“=”)7,溶液中离子浓度由大到小的顺序为______________。已知Ksp(BaA)=1.8×10-10,向该溶液中加入10 mL 1 mol·L-1BaCl2溶液,混合后溶液中的Ba2+浓度为________mol·L-1。
(3)若有下列三种溶液:①0.01 mol·L-1的H2A溶液;②0.01 mol·L-1的NaHA溶液;③0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合,则三种情况下,溶液中c(H2A)最大的是____________;pH由大到小的顺序为______________。
(4)若溶液M由pH=3的H2A溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,混合溶液中![]() =104,V1与V2的大小关系为________(填“V1大于V2”“V1等于V2”“V1小于V2”或“均有可能”)。
=104,V1与V2的大小关系为________(填“V1大于V2”“V1等于V2”“V1小于V2”或“均有可能”)。
【答案】H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2->c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+)5.4×10-10③②>③>①均有可能
H++A2->c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+)5.4×10-10③②>③>①均有可能
【解析】
(1)因为同时存在的分子有H2O、H2A,则H2A为弱酸;(2)等体积混合生成Na2A,为强碱弱酸盐,水解显碱性,A2-离子水解以第一步为主;(3)(1)弱酸电离,(2)中HA-水解生成分子,(3)中等体积混合为等量的NaCl、NaHA、H2A,抑制弱酸的电离;(4)混合溶液c(H+)/ c(OH-)=104, c(H+)=10-5mol/L,溶液显酸性,则酸过量,以此分析。
(1)因为同时存在的分子有H2O、H2A,则H2A为二元弱酸,电离方程式为H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-,因此,本题正确答案是: H2A
H++A2-,因此,本题正确答案是: H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-
H++A2-
(2)NaHA与NaOH以等物质的量反应后生成Na2A,由于A2-水解使溶液显碱性,所以pH>7;Na2A溶液中离子浓度的大小顺序为c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+);由离子方程式Ba2++A2-=BaA↓可得:反应后A2-过量0.01 mol,溶液中c(A2-)=![]() =
=![]() mol·L-1,根据BaA的Ksp可得:c(Ba2+)=
mol·L-1,根据BaA的Ksp可得:c(Ba2+)=![]() mol/L=5.4×10-10mol/L。本题答案为:>; c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) ;5.4×10-10。
mol/L=5.4×10-10mol/L。本题答案为:>; c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) ;5.4×10-10。
(3)③中溶质为物质的量浓度均为0.01 mol/L的NaCl、NaHA、H2A。NaHA、H2A相互抑制,弱酸电离程度较小,酸式酸根离子水解程度更小,所以这三种溶液中c(H2A)最大的为③;①为酸溶液,pH最小,②为盐溶液,③为酸和盐的混合溶液,所以pH③<②,则这三种溶液pH大小顺序是②>③>①。本题答案为:③ . ②>③>① 。
(4)混合溶液![]() =104,说明溶液呈酸性,则酸过量,H2A为弱酸,pH=3的H2A溶液与pH=11的NaOH溶液混合时酸的浓度大于碱的浓度,则二者体积关系不确定,大于、小于或等于都可能酸过量,因此,本题正确答案是:均有可能。
=104,说明溶液呈酸性,则酸过量,H2A为弱酸,pH=3的H2A溶液与pH=11的NaOH溶液混合时酸的浓度大于碱的浓度,则二者体积关系不确定,大于、小于或等于都可能酸过量,因此,本题正确答案是:均有可能。


科目:高中化学 来源: 题型:
【题目】下列对化学反应的认识正确的是( )
A. 化学反应过程中,分子的种类和数目一定发生改变
B. 如果某化学反应的ΔH和ΔS均小于0,则反应一定能自发进行
C. 化学反应过程中,一定有化学键的断裂和形成
D. 放热反应的反应速率一定比吸热反应的反应速率快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
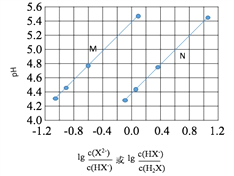
A. Ka2(H2X)的数量级为10-6
B. 曲线N表示pH与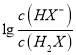 的变化关系
的变化关系
C. NaHX溶液中c(H+)>c(OH-)
D. 当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向CuSO4溶液中加入H2O2溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(Cu2O),继续加入H2O2溶液,红色浑浊又变为蓝色溶液,这个反应可以反复多次。下列关于上述过程的说法不正确的是
A. Cu2+是H2O2分解反应的催化剂 B. H2O2只表现了氧化性
C. H2O2的电子式为: ![]() D. 发生了反应Cu2O + H2O2+4H+=2Cu2++3H2O
D. 发生了反应Cu2O + H2O2+4H+=2Cu2++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是
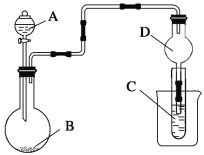
A. 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
B. 若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解
D. 若A为浓硫酸,B为Na2SO3固体,C中盛石蕊试液,则C中溶液先变红后褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应:2A(g)+3B(g)![]() C(g)+4D(g),速率最快的是( )
C(g)+4D(g),速率最快的是( )
A. v(C)=0.1mol·L-1·s-1 B. v(B)=4.0 mol·L-1·min-1
C. v(A)=2.0mol·L-1·min-1 D. v(D)=0.3mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在第n电子层中,当它作为原子的最外层时,其最多容纳的电子数与第(n-1)层相同;当它作为原子的次外层时,其最多容纳的电子数比(n-1)层多10个,则对此电子层的判断正确的是( )
A.必为K层B.必为L层C.必为M层D.可为任意层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质或结构在元素组成上最相似的一组是
A. ATP、DNA、磷脂
B. 甲状腺激素、生长激素、性激素
C. 核糖、核糖体、核糖核酸
D. 淀粉、淀粉酶、控制淀粉酶合成的DNA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒(Se)是人体健康必需的一种微量元素。已知Se的原子结构示意图如下,下列说法正确的是
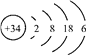
A. 该元素处于第四周期第IVA族B. SeO2既有氧化性又有还原性
C. 该原子的质量数为34D. 酸性:HBrO4 <H2SeO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com