工业上制备单质碘的方法之一是从碘酸盐开始的.第一步先用适量的亚硫酸氢盐将碘酸盐还原成碘化物,离子方程式为:IO3-+3HSO3-?I-+3SO42-+3H+.第二步将第一步得到的酸性碘化物溶液再跟适量的碘酸盐溶液合,发生反应析出了碘.请回答下列各小题:
(1)第二步发生反应的离子方程式是______.
(2)①配平下列离子方程式:
______Fe(OH)3+______ClO-+______OH-→______FeO4n-+______Cl-+______H2O
②已知有0.03mol Fe(OH)3参加了反应,共转移了0.09mol电子,则n=______,FeO4n- 中铁的化合价为______.
③根据(1)、(2)推测FeO4n- 能和下列______(填序号)物质反应.
A.KMnO4 B.SO2 C.H2S D.O2.
解:(1)由题意知,反应物有氢离子、碘离子、碘酸根离子,生成物有碘单质,再根据原子守恒判断生成物还有水,再根据得失电子数相等配平方程式.
故答案为:5 I-+IO3-+6H+=3 I2 +3H2O
(2)①元素的化合价变化分别是:Fe元素由Fe(OH)3中+3价变成-FeO4n中+(8-n)价,失去电子数为(5-n)个;
Cl元素由ClO-中的+1价变成Cl-中的-1价,得电子数为2个;根据氧化还原反应中得失电子守恒,其最小公倍数为
2(5-n),所以其计量数分别是2; (5-n); 2n;2;( 5-n );(n+3)
故答案为:2; (5-n); 2n;2;( 5-n );(n+3)
②2 Fe(OH)3 +(5-n)ClO-+2n OH-=2 FeO4n-+(5-n) Cl-+(3+n) H2O 转移电子数
2 2(5-n)
0.03mol 0.09mol
所以n=2
FeO4n-中Fe的化合价为8-2=+6,
故答案为:2;+6
③FeO4n-中Fe的化合价为+6价,为高价态,具有强氧化性,能和强还原性的物质反应.SO2和H2SD3具有还原性,故选BC
分析:(1)根据题意判断反应物、生成物,再根据得失电子守恒配平方程式.
(2)①根据氧化还原反应中得失电子数相等配平方程式.
②根据物质的量之比等于其计量数之比判断;
点评:氧化还原反应方程式配平:1、配平原则:在氧化还原反应元素间得失电子总数(或化合价升降总数)相等.
2、配平方法:一标、二找、三定、四平、五查



 NH3↑+H2O
NH3↑+H2O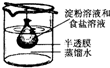 将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示),2min后分别取袋内和烧杯内液体进行实验.下列说法正确的是
将10mL淀粉胶体和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图所示),2min后分别取袋内和烧杯内液体进行实验.下列说法正确的是