
 2013年,“雾霾”成为年度关键词.近年来,对“雾霾”的防护与治理成为越来越重要的环境问题和社会问题.雾霾主要由二氧化硫、氮氧化物和可吸入颗粒物这三项组成.
2013年,“雾霾”成为年度关键词.近年来,对“雾霾”的防护与治理成为越来越重要的环境问题和社会问题.雾霾主要由二氧化硫、氮氧化物和可吸入颗粒物这三项组成.分析 (1)C3H6催化还原尾气中的NO气体,可以得到无毒的气体氮气和二氧化碳;
(2)②×2+③×2-①得到2NO(g)+2CO(g)?N2(g)+2CO2(g),据此计算反应的焓变;
(3)电解反应中阴极上发生得电子的还原反应,根据反应原理来回答书写;
(4)①反应平衡常数K=$\frac{产物平衡浓度系数次幂之积}{反应物平衡浓度系数次幂之积}$;
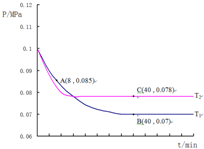
②结合化学三行计算列式,依据图中A点时,气体物质的量0.085,依据开始和A点气体物质的量之比列式计算,转化率=$\frac{变化量}{起始量}$×100%;
③图中B点,依据化学三行列式计算用平衡分压代替平衡浓度计算,分压=总压×物质的量分数计算SO2催化氧化反应在图中B点的压强平衡常数;
④先拐先平温度高,达到平衡所需时间短,温度越高反应速率越大.
解答 解:(1)C3H6催化还原尾气中的NO气体,可以得到无毒的气体氮气和二氧化碳,即2C3H6+18NO=6CO2+6H2O+9N2;故答案为:2C3H6+18NO=6CO2+6H2O+9N2;
(2))②×2+③×2-①得到2NO(g)+2CO(g)?N2(g)+2CO2(g),反应的焓变=2(+110.5kJ•mol-1)+2(-393.5kJ•mol-1)-(180.5kJ•mol-1)=-746.5kJ•mol-1,故答案为:-746.5kJ•mol-1;
(3)电解反应中阴极上发生得电子的还原反应,2HSO3-+2H++2e-=S2O42-+2H2O,故答案为:2HSO3-+2H++2e-=S2O42-+2H2O;
(4)①2SO2(g)+O2(g)?2SO3,反应的平衡常数K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})c({O}_{2})}$,
故答案为:$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})c({O}_{2})}$;
②依据化学三行列式计算,设氧气消耗物质的量为x,
2SO2(g)+O2(g)?2SO3
起始量(mol) 2a a 0
变化量(mol) 2x x 2x
平衡量(mol)2a-2x a-x 2x
图中A点时,气体物质的量0.085,则$\frac{2a-2x+a-x+2x}{2a+a}$=$\frac{0.085}{0.1}$,x=0.45a
SO2的转化率=$\frac{0.45a×2}{2a}$×100%=45%,
故答案为:45%;
③图中B点,依据化学三行列式计算,设氧气消耗物质的量为y,
2SO2(g)+O2(g)?2SO3
起始量(mol) 2a a 0
变化量(mol) 2y y 2y
平衡量(mol)2a-2y a-y 2y
B点气体物质的量为 0.007,则$\frac{2a-2y+a-y+2y}{2a+a}$=$\frac{0.07}{0.1}$,y=0.9a,
平衡常数K=($\frac{(0.007×\frac{1.8}{0.2a+0.1a+1.8a})^{2}}{(0.007×\frac{0.2a}{0.2a+0.1a+1.8a})^{2}×(0.007×\frac{0.1a}{0.2a+0.1a+1.8a})}$)=24300(MPa)-1,
故答案为:24300(MPa)-1;
④图象分析可知,先拐先平温度高则T1<T2,C点是平衡状态,A点反应未达到平衡状态,其中C点的正反应速率vC(正)与A点的逆反应速率vA(逆)的大小关系为vC(正)>vA(逆)
故答案为:<,>.
点评 本题考查了化学平衡、化学反应速率影响因素的分析应用,图象变化和数值的计算是解题关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | N2H4(g)+O2(g)═N2(g)+2H2O(g);△H=+534 kJ•mol-1 | |
| B. | N2H4(l)+O2(g)═N2(g)+2H2O(g);△H=-534 kJ•mol-1 | |
| C. | N2H4(g)+O2(g)═N2(g)+2H2O(l);△H=-534 kJ•mol-1 | |
| D. | N2H4(g)+O2(g)═N2(g)+2H2O(l);△H=-622 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 请根据所学化学反应原理,解决以下问题:
请根据所学化学反应原理,解决以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C10H19O | |
| B. | 同分异构体可能属于醛类、酮类或酚类 | |
| C. | 能发生取代、氧化、还原反应 | |
| D. | 与氢气加成后的产物有4种一氯化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2 g CH30H含有的化学键数为0.4NA | |
| B. | 0.1 mol FeCl3水解制得的Fe( OH)3胶体中胶粒数是0.1NA | |
| C. | 标准状况下,2.24 L Cl2溶于足量水,转移的电子数为0.1NA | |
| D. | 0.2 g D216O中含有的质子数、中子数和电子数均为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如所示:
是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如所示:
 $→_{△}^{H_{2}O/H+}$
$→_{△}^{H_{2}O/H+}$
 .
. $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +H2O.
+H2O. ,与D互为同分异构体且含有碳碳双键的苯的二取代物有6种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式是
,与D互为同分异构体且含有碳碳双键的苯的二取代物有6种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式是 (任写一种).
(任写一种). )的
)的查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol-OH(羟基)与l mol NH4+中所含电子数均为10NA | |
| B. | 25℃时,100 mL pH=l的稀硫酸中,含有的H+数目为0.01 NA | |
| C. | 室温下,1 L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1 NA | |
| D. | 标准状况下,2.24LNO2和N2O4混合气体中含0.2 NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com