
| A. | 氨水 | B. | NaOH溶液 | C. | NaCl溶液 | D. | NH4Cl溶液 |
分析 要使AlCl3溶液中铝元素完全沉淀出来,应与碱反应将其转化为氢氧化铝沉淀,氢氧化铝是两性氢氧化物,溶于强酸与强碱,所以适宜选用弱碱.
解答 解:A、氨水为弱碱与AlCl3溶液反应生成氢氧化铝沉淀,不能溶解氢氧化铝,使Al元素完全沉淀,故A选;
B、氢氧化钠是强碱,氢氧化钠过量会溶解氢氧化铝,生成偏铝酸盐,使Al元素不能完全沉淀,故B不选;
C、氯化钠溶液不和氯化铝溶液反应,不能使Al元素沉淀,故C不选;
D、氯化铵溶液水解显酸性,氯化铝溶液水解显酸性,二者不发生反应,故D不选.
故选A.
点评 本题考查铝及其化合物的性质,难度不大,注意氧化铝、氢氧化铝的两性及氢氧化铝的制备必须使用弱碱.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:选择题
 常温下,0.2mol•L-1的一元酸HCl与等浓度的MOH溶液等体积混合后,所得溶液中部分微粒组成及浓度如图所示,下列说法正确的是( )
常温下,0.2mol•L-1的一元酸HCl与等浓度的MOH溶液等体积混合后,所得溶液中部分微粒组成及浓度如图所示,下列说法正确的是( )| A. | MOH为强碱 | |
| B. | 该混合液pH=7 | |
| C. | 该混合溶液中:c(Cl-)=c(M+) | |
| D. | 图中X表示M+,Y表示H+,Y表示MOH,R表示OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 戊二醛的分子式为C5H8O2,符合此分子式的二元醛有5种 | |
| B. | 戊二醛不能使酸性高锰酸钾溶液褪色 | |
| C. | 戊二醛经催化氧化可以得到的戊二酸有4种同分异构体 | |
| D. | 1mol的戊二醛与足量的银氨溶液反应,最多可得2mol单质银 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$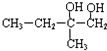 +2NaBr,反应类型是取代反应.
+2NaBr,反应类型是取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价.如图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )
高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价.如图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )| A. | 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2- | |
| B. | 晶体中每个K+周围有8个O2-,每个O2-周围有8个K+ | |
| C. | 晶体中与每个K+距离最近的K+有8个 | |
| D. | 晶体中,0价氧与-2价氧的数目比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 陈述Ⅰ | 陈述Ⅱ | |
| A | NaHCO3为强碱弱酸盐,只存在水解平衡 | NaHCO3溶液显碱性 |
| B | HCL与Na2CO3溶液反应生成CO2 | 用饱和NaCO3溶液除去CO2中的少量HCl |
| C | Cl2使润湿的有色布条褪色,而干燥的布条不褪色 | 次氯酸的氧化性比氯气的强 |
| D | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 是生漆的主要成分,黄色能溶于有机溶剂中.生漆涂在物体表面,能在空气中干燥转变为黑色漆膜,下列有关其化学性质的叙述不正确的是( )
是生漆的主要成分,黄色能溶于有机溶剂中.生漆涂在物体表面,能在空气中干燥转变为黑色漆膜,下列有关其化学性质的叙述不正确的是( )| A. | 能发生氧化反应 | B. | 与FeCl3溶液发生显色反应 | ||
| C. | 能发生取代反应和加成反应 | D. | 与足量浓溴水反应时,消耗溴4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| I1 | I2 | I3 | I4 | … | |
| R | 740 | 1 500 | 7 700 | 10 500 |
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com